9291在什么时候上市的呢?

我国首个获批的第三代肺癌药物奥希替尼9291正式在国内上市了,用于治疗EGFR T790M突变阳性的局部晚期或转移性非小细胞肺癌,据悉,奥希替尼9291国内售价为每月5.1万(80mg*30片)(美国原研药的售价:5.7万$一盒(80mg*30粒)。奥希替尼9291是阿斯利康公司研发的第三代口服、不可逆的选择性EGFR突变抑制剂肺癌药物,是全球第一个上市,也是我国首个获批的用于EGFR T790M突变阳性的局部晚期或转移性非小细胞肺癌的肿瘤药物。2015年11月,奥希替尼9291获FDA批准在美国首先上市,从临床试验到上市许可仅历时两年半,是阿斯利康史上研发速度最快的新药项目。
化合物奥希替尼9291于2013年5月首次开始用于临床试验,基于临床前的研究结论,采用20 mg,每日一次的治疗剂量,第一位患者是一名来自韩国的亚裔57岁女性,于2011年被诊断为四期EGFR非小细胞肺癌,经化合物9的治疗后,肿瘤缩小了39.7%。第二位患者是一名来自英国的57岁白人女性,于2010年被诊断为四期肺腺癌,经由化合物9的治疗后,肿瘤缩小了38%,症状得到了明显的改善,在长达9个月的治疗中,两位患者都保持对化合物9的持续应答反应,而且未观察到明显的血糖异常现象!在剂量递增试验中,80 mg每日一次的剂量表现出最大的肿瘤抑制活性,并显示对脑转移癌的潜在活性,并且相关副作用效果最小,因此最终采用80 mg的单日一次的治疗剂量。基于上述一期临床的研究结果,2014年4月,FDA授予奥希替尼9291“突破性疗法”!
2016年9月,国家食品药品监督管理总局基于晚期肺癌患者的临床急需及奥希替尼9291与现有治疗相比明显的治疗优势,将其列入优先审评名单,并予以加速批准,2017年3月24日,奥希替尼9291正式在我国获批上市,瞬间成为众多肺癌患者翘首期盼的关注对象。
参考资料: FDA说明书更新于2024年09月25日,FDA说明书网址:https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=208065
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
药品信息

- 奥希替尼(Osimertinib)的药代动力学奥希替尼(Osimertinib、Tagrisso、泰瑞沙)是一种口服的第三代表...[ 详情 ]推荐指数:692026-03-06 14:33:42
- Tagrisso(奥希替尼)联合化疗获美国批准用于EGFR突变晚期非小细胞肺癌患者2024年2月19日电——阿斯利康旗下的Tagrisso(通用名:奥希替尼)已获...[ 详情 ]推荐指数:3442025-12-31 14:49:29
- Tagrisso(奥希替尼)获美国批准用于不可切除Ⅲ期EGFR突变肺癌患者英国剑桥,2024年9月26日电——阿斯利康旗下的Tagrisso(通用名:奥希...[ 详情 ]推荐指数:3052025-12-31 14:12
- 奥希替尼(Osimertinib)在国内上市了吗?奥希替尼(Osimertinib)是一种第三代EGFR酪氨酸激酶抑制剂,由英国阿...[ 详情 ]推荐指数:5302025-09-28 16:09:05
- 奥希替尼(Osimertinib)纳入医保了吗?奥希替尼(Osimertinib)是第三代EGFR酪氨酸激酶抑制剂(TKI),为...[ 详情 ]推荐指数:6322025-09-28 16:09:16
- 靶向药奥希替尼(Osimertinib),泰瑞沙,Tagrisso的详细说明书奥希替尼(Osimertinib)适用于多种非小细胞肺癌(NSCLC)的治疗,在...[ 详情 ]推荐指数:5742025-08-22 15:13:40
- 靶向药奥希替尼(Osimertinib)的中文说明书奥希替尼(Osimertinib)自2015年在美国获得FDA批准上市以来,在全...[ 详情 ]推荐指数:9082025-08-20 14:36:39
- 奥希替尼(Osimertinib)的副作用:严重不良反应,常见副作用,副作用管理奥希替尼(Osimertinib)是一种靶向药,属于第三代EGFR(表皮生长...[ 详情 ]推荐指数:6532025-08-20 14:33:21
- 奥希替尼的用药注意事项有哪些奥希替尼用药需严格遵循注意事项,涉及心肺监测、剂量调整、特殊人群用药等多方面要求...[ 详情 ]已帮助1185人2025-08-27 11:25:05
- 奥希替尼的注意事项都有哪些?奥希替尼的注意事项涵盖肺部、心脏、皮肤等多系统风险,需重点监测间质性肺病、QT间...[ 详情 ]已帮助1179人2025-08-27 11:20:44
- 奥希替尼药物相互作用全解析奥希替尼(Osimertinib)的药物相互作用主要涉及转运蛋白系统、QT间期延...[ 详情 ]已帮助1243人2025-08-26 17:19:03
- 奥希替尼的用法用量奥希替尼(Osimertinib)的标准剂量为每日80mg口服,适用于不同阶段的...[ 详情 ]已帮助1186人2025-08-26 17:16:33
- 奥希替尼的特殊人群用药奥希替尼(Osimertinib)作为第三代EGFR-TKI抑制剂,其特殊人群用...[ 详情 ]已帮助1204人2025-08-26 17:08:48
- 奥希替尼的药代动力学奥希替尼是一种用于治疗非小细胞肺癌的靶向药物,其药代动力学特性对于临床用药具有重...[ 详情 ]已帮助1197人2025-08-26 16:47:47
- 奥希替尼的适应靶点奥希替尼是一种针对表皮生长因子受体(EGFR)特定基因突变的靶向治疗药物,主要针...[ 详情 ]已帮助1167人2025-08-26 16:27:09
- 奥希替尼的主要成分奥希替尼的活性成分是Osimertinib,以独特的靶向作用对特定的非小细胞肺癌...[ 详情 ]已帮助1165人2025-08-26 14:50:26
- PM8002联合紫杉醇对比化疗二线治疗小细胞肺癌[适 应 症]小细胞肺癌[试验分期]Ⅱ期
- ES102联合特瑞普利单抗治疗晚期非小细胞肺癌[适 应 症]非小细胞肺癌[试验分期]Ⅱ期
- 比较Sigvotatug Vedotin与多西他赛治疗既往经治的非小细胞肺癌的研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- QL2107或Keytruda®联合化疗治疗转移性非鳞状非小细胞肺癌的临床研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- LM-299注射液单药或联合其它抗肿瘤药物治疗晚期实体瘤[适 应 症]实体瘤[试验分期]Ⅰ期
- SH-1028片对比安慰剂用于非小细胞肺癌辅助治疗[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
做您身边的贴心健康咨询管家

了解医药信息 关注临床动态
- 1美洛加巴林(Tarlige)的适应症与用法用量已帮助3人2026-03-25 17:04:13
- 2阿尼鲁单抗(Saphnelo)的疗效已帮助3人2026-03-25 17:50
- 3靶向药坦罗莫司(Temsirolimus)的功效与作用已帮助4人2026-03-25 17:05:08
- 4奥维昔巴特(Bylvay)的注意事项和药物相互作用已帮助3人2026-03-25 17:35
- 5奥维昔巴特(Bylvay)是治疗什么疾病的已帮助4人2026-03-25 17:26
- 6奥维昔巴特(Bylvay)的副作用如何缓解已帮助5人2026-03-25 17:15
- 7奥维昔巴特(Bylvay)的用药注意事项已帮助4人2026-03-25 17:04
- 8奥维昔巴特(Bylvay)的功效与作用已帮助4人2026-03-25 16:59
- 9非诺贝特片(Lipidil)国内能买到吗?在哪能买到?已帮助4人2026-03-25 16:43
- 10非诺贝特片(Lipidil)的用药指南已帮助4人2026-03-25 16:43
- 11非诺贝特片(Lipidil)怎么购买已帮助8人2026-03-25 16:26
- 122026年非诺贝特片(Lipidil)最新价格是多少钱一盒?已帮助5人2026-03-25 15:59
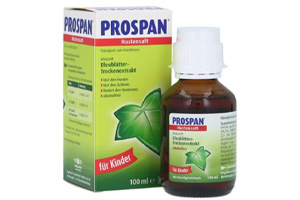 Prospan糖浆(Prospan Cough Liquid)用于缓解慢性炎性支气管疾病(如慢性支气管炎)的症...[ 详情 ]
Prospan糖浆(Prospan Cough Liquid)用于缓解慢性炎性支气管疾病(如慢性支气管炎)的症...[ 详情 ]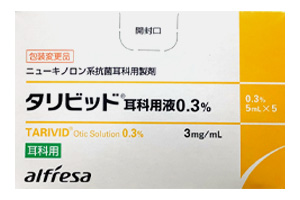 氧氟沙星耳科用液(Tarivid)适用于治疗对氧氟沙星敏感的致病菌感染所致的外耳炎...[ 详情 ]
氧氟沙星耳科用液(Tarivid)适用于治疗对氧氟沙星敏感的致病菌感染所致的外耳炎...[ 详情 ]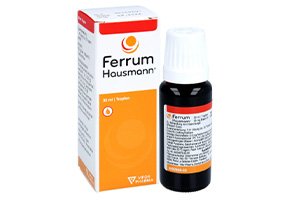 Ferrum Hausmann铁剂治疗铁缺乏性贫血。妊娠期铁缺乏的治疗及预防性用药...[ 详情 ]
Ferrum Hausmann铁剂治疗铁缺乏性贫血。妊娠期铁缺乏的治疗及预防性用药...[ 详情 ] 复代文(Co-Diovan)适用于18岁及以上,单药治疗(单用缬沙坦或氢氯噻...[ 详情 ]
复代文(Co-Diovan)适用于18岁及以上,单药治疗(单用缬沙坦或氢氯噻...[ 详情 ]