gemtuzumab ozogamicin纳入医保了吗?

gemtuzumab ozogamicin是一款在美国上市的治疗白血病的药物,那么很多患者就会想知道这款药物在国内上市了吗?gemtuzumab ozogamicin纳入医保了吗?今天咱们就来详细看一下。
gemtuzumab ozogamicin是由抗CD33蛋白单克隆抗体和卡奇霉素两部分组成的抗体偶联药物,前者可以与CD33蛋白结合,发挥定位的作用;后者是具有强毒性的细胞毒素,发挥子弹的作用。
2017年9月1日,美国食品和药物管理局批准gemtuzumab ozogamicin用于治疗成人新确诊的CD33阳性急性髓细胞白血病(AML)、成人复发或难治性AML和2岁及儿科患者的AML。gemtuzumab ozogamicin已在日本上市,用于被认为不适合其他细胞毒化疗的复发性或难治性CD33阳性AML患者。 英国国立健康与临床优化研究所(NICE)最终评估决定推荐辉瑞gemtuzumab ozogamicin与化疗联合使用,用于治疗以前未治疗的、全新CD33阳性的急性髓细胞白血病。
但目前国内gemtuzumab ozogamicin还没有上市,也就无法纳入医保。
gemtuzumab ozogamicin在不良反应方面:
1、全身反应:腹痛、乏力、背痛、寒战、发热、头痛、败血症、肿瘤溶解综合征。
2、循环系统:低血压、高血压、心律失常。
3、消化系统:食欲不振、恶心、呕吐、便秘、腹泻、腹胀、消化不良、胃炎、肝毒性、肝静脉血栓。
4、血液系统;骨髓抑制(较严重)、贫血、血小板减少、出血(鼻出血、脑出血、瘀斑、颅内出血、血尿、阴道出血)、弥漫性血管内凝血。
5、代谢系统:低钾血症、低镁血症、乳酸脱氢酶升高、高血糖。
6、肌肉骨骼:关节痛。
7、神经系统:抑郁、失眠、眩晕。
8、呼吸系统:呼吸困难、低氧血症、肺炎、咳嗽加重、咽炎、鼻炎。
9、皮肤及附属物:单纯疱疹、皮疹、局部反应、周围水肿。
在一项纳入271例新确诊CD33+成人急性髓性白血病患者的试验中,gemtuzumab ozogamicin的疗效得到了证实。该研究评估了患者的无事件生存期,结果发现gemtuzumab ozogamicin+化疗的中位无事件生存期显著长于化疗组(17.3 vs 9.5个月)。可见gemtuzumab ozogamicin虽然有不良反应,但是治疗效果还是很好的。
以上就是gemtuzumab ozogamicin医保的内容,希望可以帮助到您!
参考资料: FDA说明书更新于2020年6月16日,FDA说明书网址:https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=761060
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
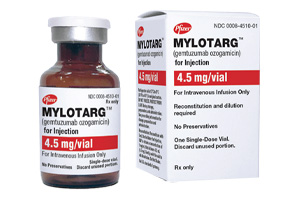
药品信息

- 吉妥单抗的副作用如何缓解吉妥单抗在发挥抗肿瘤作用的同时可能引发多种不良反应,了解这些副作用的表现形式、掌...[ 详情 ]推荐指数:4382025-07-15 16:11:54
- 吉妥单抗的适应症吉妥单抗是一种靶向CD33抗原的抗体药物偶联物,通过特异性结合白血病细胞表面的C...[ 详情 ]推荐指数:5262025-07-15 15:26
- 吉妥单抗的用法用量?吉妥单抗是一种靶向CD33的抗体偶联药物,主要用于CD33阳性的急性髓系白血病,...[ 详情 ]推荐指数:4432025-07-15 15:17
- 吉妥单抗的副作用与注意事项吉妥单抗是一种靶向CD33抗原的抗体药物偶联物,用于治疗CD33阳性急性髓系白血...[ 详情 ]推荐指数:3952025-07-15 14:31
- 吉妥单抗有几种规格?多少钱?导读:吉妥单抗在治疗CD33阳性急性髓细胞白血病(AML)方面有一定的疗效,根据...[ 详情 ]推荐指数:7042025-02-13 14:43
- 吉妥单抗有哪几个版本?分别多少钱?导读:吉妥单抗(Mylotarg)是一种用于治疗急性髓系白血病(AML)的靶向药...[ 详情 ]推荐指数:7612025-02-13 14:30:24
- 吉妥单抗多少钱一盒?在哪里购买?导读:吉妥单抗是一种用于治疗CD33阳性急性髓细胞白血病(AML)的药物,其价格...[ 详情 ]推荐指数:7112025-02-13 13:49
- 吉妥单抗能有效治病吗?导读:吉妥单抗是一种用于治疗CD33阳性急性髓细胞白血病(AML)的靶向药物,其...[ 详情 ]推荐指数:6572025-08-12 13:45:25
- 孕妇可以使用吉妥单抗吗?孕妇不可以使用吉妥单抗。孕妇不能使用吉妥单抗。根据药物说明书和相关研究,吉妥单抗...[ 详情 ]已帮助877人2025-02-12 10:27
- 吉妥单抗有效期是多长时间?吉妥单抗有效期通常是24个月。吉妥单抗有效期取决于其储存条件和生产日期,药品的有...[ 详情 ]已帮助898人2025-02-12 10:26
- 吉妥单抗不同版本一盒的最新价格公布奥佐米星也就是吉妥单抗,目前了解到土耳其版的吉妥单抗价格大约是4818美元一盒,...[ 详情 ]已帮助797人2025-02-14 13:36:48
- 吉妥单抗正品有合适的购买方式吗?吉妥单抗正品有合适的购买方式,比较常见的购买方式主要有以下几种。1、医院药房:患...[ 详情 ]已帮助766人2025-02-14 13:35:46
- 吉妥珠单抗价格一览目前并没有了解到吉妥珠单抗有仿制药,也无法得知其价格。吉妥珠单抗原研药价格较为昂...[ 详情 ]已帮助783人2025-08-18 11:48:48
- 吉妥单抗全新购买方式一览奥佐米星吉妥单抗可参考以下几种。1、医院药房:患者可前往吉妥单抗上市国家或地区,...[ 详情 ]已帮助801人2025-02-14 13:32:52
- 吉妥单抗最新公布价格表目前了解到土耳其版吉珠单抗的价格大约是4803美元一盒,价格比较昂贵,需要患者自...[ 详情 ]已帮助970人2025-02-13 13:36:44
- 吉妥单抗全网公布的2024年的最新价格吉妥单抗全网公布的2024年的最新价格比较昂贵,目前了解到出口到土耳其版的吉妥单...[ 详情 ]已帮助757人2025-02-17 15:26:08
- PM8002联合紫杉醇对比化疗二线治疗小细胞肺癌[适 应 症]小细胞肺癌[试验分期]Ⅱ期
- ES102联合特瑞普利单抗治疗晚期非小细胞肺癌[适 应 症]非小细胞肺癌[试验分期]Ⅱ期
- 比较Sigvotatug Vedotin与多西他赛治疗既往经治的非小细胞肺癌的研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- QL2107或Keytruda®联合化疗治疗转移性非鳞状非小细胞肺癌的临床研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- LM-299注射液单药或联合其它抗肿瘤药物治疗晚期实体瘤[适 应 症]实体瘤[试验分期]Ⅰ期
- SH-1028片对比安慰剂用于非小细胞肺癌辅助治疗[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
做您身边的贴心健康咨询管家

了解医药信息 关注临床动态
- 1坦罗莫司(Temsirolimus)的用药指南已帮助12人2026-03-27 17:46
- 2吉瑞替尼(Gilteritinib)的适应症已帮助10人2026-03-27 17:46
- 3哌柏西利(palbociclib)用药副作用已帮助11人2026-03-27 17:46
- 4雷洛昔芬(Raloxifene)的副作用如何缓解已帮助8人2026-03-27 17:45:56
- 5雷洛昔芬(Raloxifene)的用药注意事项已帮助10人2026-03-27 16:26:28
- 6雷洛昔芬(Raloxifene)的功效与作用已帮助9人2026-03-27 16:26:38
- 7卡比多巴左旋多巴缓释胶囊(Crexont)国内能买到吗?在哪能买到?已帮助10人2026-03-27 17:10:52
- 8卡比多巴左旋多巴缓释胶囊(Crexont)的用药指南已帮助11人2026-03-27 17:04:45
- 9卡比多巴左旋多巴缓释胶囊(Crexont)的用法用量已帮助9人2026-03-27 16:26
- 10卡比多巴左旋多巴缓释胶囊(Crexont)怎么购买已帮助9人2026-03-27 16:37:28
- 112026年卡比多巴左旋多巴缓释胶囊(Crexont)最新价格是多少钱一盒?已帮助9人2026-03-27 16:13
- 12卡比多巴左旋多巴缓释胶囊(Crexont)国内价格是多少已帮助10人2026-03-27 16:09
 盐酸二甲双胍缓释片(Glucophage XR)作为饮食和运动的辅助治疗,用于改善成人2型糖尿病...[ 详情 ]
盐酸二甲双胍缓释片(Glucophage XR)作为饮食和运动的辅助治疗,用于改善成人2型糖尿病...[ 详情 ] 格列本脲(Euglucon)仅适用于胰岛素非依赖型、具备一定胰岛功能、无酮症...[ 详情 ]
格列本脲(Euglucon)仅适用于胰岛素非依赖型、具备一定胰岛功能、无酮症...[ 详情 ] Prospan糖浆(Prospan Cough Liquid)用于缓解慢性炎性支气管疾病(如慢性支气管炎)的症...[ 详情 ]
Prospan糖浆(Prospan Cough Liquid)用于缓解慢性炎性支气管疾病(如慢性支气管炎)的症...[ 详情 ] 氧氟沙星耳科用液(Tarivid)适用于治疗对氧氟沙星敏感的致病菌感染所致的外耳炎...[ 详情 ]
氧氟沙星耳科用液(Tarivid)适用于治疗对氧氟沙星敏感的致病菌感染所致的外耳炎...[ 详情 ]