gemtuzumab ozogamicin的说明书

2017年9月1日,美国食品和药物管理局批准吉妥珠单抗(Mylotarg、Gemtuzumab ozogamicin)用于治疗成人新确诊的CD33阳性急性髓细胞白血病(AML)、成人复发或难治性AML和2岁及儿科患者的AML。对于新诊断的AML患者,Gemtuzumab ozogamicin可与柔红霉素和阿糖胞苷联合使用,或用于某些成人和儿科患者的独立治疗。
Gemtuzumab ozogamicin注意事项:
出血
在MYLOTARG治疗期间,可能发生具有致命性的血小板计数降低的情况,且由此相关的并发症可能包括出血或失血事件,这也可能危及生命。如果您在MYLOTARG治疗期间须出现出血/出血的体征和症状,请及时告诉医生。若出现严重出血或失血的情况,您的医生可能会中断给药或永久性停用MYLOTARG。
输液相关反应
在输注MYLOTARG期间或之后24小时内,可发生危及生命或致命的输液相关反应,包括发烧、发冷、低血压、心动过速、缺氧和呼吸衰竭。如果您出现输液相关反应的症状和体征,包括发烧,发冷,皮疹或呼吸困难等症状,请尽快联系您的医生。在输注MYLOTARG之前,须进行预先注射。在输液期间,您的医生会监测您的生命体征。如果你出现输液反应,尤其是呼吸困难、支气管痉挛或低血压者,您的医生会应立即中断输液。在输注期间和结束至少1小时内,您应该留院观察,一直到症状和症状完全消退为止。
过敏反应
若出现过敏反应症状,包括严重的呼吸道症状或临床显着的低血压,您的医生会立即停止给药。
怀孕和母乳喂养
建议具有生殖潜力的男性和女性在MYLOTARG治疗期间使用有效避孕措施,并在最后一次给药后,至少继续分别使用3个月和6个月的有效避孕措施。建议有生育潜力的女性在接受MYLOTARG时避免怀孕。如果您在接受MYLOTARG治疗期间发现自己怀孕或怀疑自己怀孕了,请及时与医生联系。由于母乳喂养婴儿可能出现不良反应,因此在MYLOTARG治疗期间和最终剂量后至少1个月内,女性不应进行母乳喂养。
gemtuzumab ozogamicin副作用:
最常见的不良反应(大于15%)是出血,感染,发烧,恶心,呕吐,便秘,头痛,AST增加,谷丙转氨酶升高,皮疹和粘膜炎。
严重的副作用,包括:肝毒性,包括静脉闭塞性肝病(VOD)
在MYLOTARG治疗期间,可能出现肝脏问题,包括严重的、可致命的VOD。之前接受或将接受造血干细胞移植的患者,发生VOD的风险可能会增加。在接受MYLOTARG治疗后,同种异体造血干细胞移植出现VOD的风险也会增加。医生将会在您治疗期间应定期监测肝毒性的体征或症状,警惕包括体重快速增加、右上腹疼痛和压痛、肝肿大,和腹水在内的症状。但这些症状可能无法识别所有有风险的患者或预防肝毒性并发症。若出现肝脏问题,医生可能会中断或永久停用Gemtuzumab ozogamicin。
参考资料: FDA说明书更新于2020年6月16日,FDA说明书网址:https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=761060
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
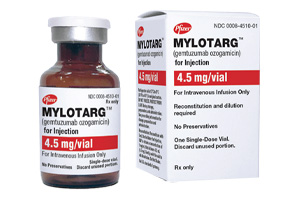
药品信息

- 吉妥单抗的副作用如何缓解吉妥单抗在发挥抗肿瘤作用的同时可能引发多种不良反应,了解这些副作用的表现形式、掌...[ 详情 ]推荐指数:4272025-07-15 16:11:54
- 吉妥单抗的适应症吉妥单抗是一种靶向CD33抗原的抗体药物偶联物,通过特异性结合白血病细胞表面的C...[ 详情 ]推荐指数:5182025-07-15 15:26
- 吉妥单抗的用法用量?吉妥单抗是一种靶向CD33的抗体偶联药物,主要用于CD33阳性的急性髓系白血病,...[ 详情 ]推荐指数:4312025-07-15 15:17
- 吉妥单抗的副作用与注意事项吉妥单抗是一种靶向CD33抗原的抗体药物偶联物,用于治疗CD33阳性急性髓系白血...[ 详情 ]推荐指数:3892025-07-15 14:31
- 吉妥单抗有几种规格?多少钱?导读:吉妥单抗在治疗CD33阳性急性髓细胞白血病(AML)方面有一定的疗效,根据...[ 详情 ]推荐指数:6912025-02-13 14:43
- 吉妥单抗有哪几个版本?分别多少钱?导读:吉妥单抗(Mylotarg)是一种用于治疗急性髓系白血病(AML)的靶向药...[ 详情 ]推荐指数:7492025-02-13 14:30:24
- 吉妥单抗多少钱一盒?在哪里购买?导读:吉妥单抗是一种用于治疗CD33阳性急性髓细胞白血病(AML)的药物,其价格...[ 详情 ]推荐指数:7032025-02-13 13:49
- 吉妥单抗能有效治病吗?导读:吉妥单抗是一种用于治疗CD33阳性急性髓细胞白血病(AML)的靶向药物,其...[ 详情 ]推荐指数:6432025-08-12 13:45:25
- 孕妇可以使用吉妥单抗吗?孕妇不可以使用吉妥单抗。孕妇不能使用吉妥单抗。根据药物说明书和相关研究,吉妥单抗...[ 详情 ]已帮助874人2025-02-12 10:27
- 吉妥单抗有效期是多长时间?吉妥单抗有效期通常是24个月。吉妥单抗有效期取决于其储存条件和生产日期,药品的有...[ 详情 ]已帮助893人2025-02-12 10:26
- 吉妥单抗不同版本一盒的最新价格公布奥佐米星也就是吉妥单抗,目前了解到土耳其版的吉妥单抗价格大约是4818美元一盒,...[ 详情 ]已帮助791人2025-02-14 13:36:48
- 吉妥单抗正品有合适的购买方式吗?吉妥单抗正品有合适的购买方式,比较常见的购买方式主要有以下几种。1、医院药房:患...[ 详情 ]已帮助764人2025-02-14 13:35:46
- 吉妥珠单抗价格一览目前并没有了解到吉妥珠单抗有仿制药,也无法得知其价格。吉妥珠单抗原研药价格较为昂...[ 详情 ]已帮助781人2025-08-18 11:48:48
- 吉妥单抗全新购买方式一览奥佐米星吉妥单抗可参考以下几种。1、医院药房:患者可前往吉妥单抗上市国家或地区,...[ 详情 ]已帮助798人2025-02-14 13:32:52
- 吉妥单抗最新公布价格表目前了解到土耳其版吉珠单抗的价格大约是4803美元一盒,价格比较昂贵,需要患者自...[ 详情 ]已帮助956人2025-02-13 13:36:44
- 吉妥单抗全网公布的2024年的最新价格吉妥单抗全网公布的2024年的最新价格比较昂贵,目前了解到出口到土耳其版的吉妥单...[ 详情 ]已帮助754人2025-02-17 15:26:08
- PM8002联合紫杉醇对比化疗二线治疗小细胞肺癌[适 应 症]小细胞肺癌[试验分期]Ⅱ期
- ES102联合特瑞普利单抗治疗晚期非小细胞肺癌[适 应 症]非小细胞肺癌[试验分期]Ⅱ期
- 比较Sigvotatug Vedotin与多西他赛治疗既往经治的非小细胞肺癌的研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- QL2107或Keytruda®联合化疗治疗转移性非鳞状非小细胞肺癌的临床研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- LM-299注射液单药或联合其它抗肿瘤药物治疗晚期实体瘤[适 应 症]实体瘤[试验分期]Ⅰ期
- SH-1028片对比安慰剂用于非小细胞肺癌辅助治疗[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
做您身边的贴心健康咨询管家

了解医药信息 关注临床动态
- 12026年舒泽曲近片(Journavx)最新价格是多少钱一盒?已帮助0人2026-03-19 15:02
- 2美国食品药品监督管理局批准米替福新(Impavido)用于治疗热带疾病利什曼病已帮助1人2026-03-19 14:39
- 3米替福新(Impavido)的副作用和不良反应已帮助1人2026-03-19 13:56:34
- 4米替福新(Impavido)的用法用量:用药指南,剂量调整,特殊人群用药已帮助1人2026-03-19 13:56:18
- 5米替福新(Impavido)中文说明书已帮助2人2026-03-19 13:56:04
- 6米替福新(Impavido)的详细说明书:作用与功效,用法用量,副作用,注意事项等已帮助2人2026-03-19 13:55:49
- 7吡托布鲁替尼(Pirtobrutinib)的适应症已帮助4人2026-03-18 17:49
- 8米托坦(Mitotane)的作用功效与用法用量已帮助5人2026-03-18 17:49
- 9沃拉西德尼(Voranigo)的适应症和用法用量已帮助4人2026-03-18 17:40
- 10舒泽曲近片(Journavx)国内价格是多少已帮助6人2026-03-18 17:37
- 11舒泽曲近片(Journavx)的注意事项和药物相互作用已帮助8人2026-03-18 17:23
- 12舒泽曲近片(Journavx)是治疗什么疾病的已帮助7人2026-03-19 09:47:20
 苯磺酸米洛沙巴林(Tarlige)主要用于成人患者的神经病理性疼痛。[ 详情 ]
苯磺酸米洛沙巴林(Tarlige)主要用于成人患者的神经病理性疼痛。[ 详情 ] 阿托伐醌(Mepron)适用于13岁及以上成人和青少年中无法耐受甲氧苄啶...[ 详情 ]
阿托伐醌(Mepron)适用于13岁及以上成人和青少年中无法耐受甲氧苄啶...[ 详情 ] 非诺贝特片(Lipidil)应在确诊为高脂血症后使用,不可作为高脂血症的预防...[ 详情 ]
非诺贝特片(Lipidil)应在确诊为高脂血症后使用,不可作为高脂血症的预防...[ 详情 ] 米替福新(Impavido)适用于12岁及以上且体重≥30公斤的成人和儿童患...[ 详情 ]
米替福新(Impavido)适用于12岁及以上且体重≥30公斤的成人和儿童患...[ 详情 ]