Actemra(tocilizumab)价格

Actemra(tocilizumab)在2013年的时候已经获批在国内上市,为国内诸多适应症患者的治疗提供了一定的帮助。由于药品规格的不同,其上市后的价格也就有所不同。目前来讲,该药的售价在1925.00$-5398.00$之间。
虽然在2019年8月罗氏就发布了公告,托珠单抗被正式纳入中国国家医保目录之中。但对于需要长期注射托珠单抗(tocilizumab)进行治疗的患者来说,医保后的价格仍然承担不起,所以国内很多患者便会选择海外购买托珠单抗,由于汇率浮动价格不固定,患者如果想要了解托珠单抗的具体价格,或是想要海外购买该药品,可以向国内靠谱的海外医疗服务机构(如医伴旅)咨询。
托珠单抗常见的不良反应主要有皮肤/软组织感染、肝损伤、高胆固醇血症、嗜中性粒细胞减少及过敏反应。当发生皮肤/软组织感染时,应进行抗生素治疗,待停药 4周感染控制后再次使用托珠单抗。当发生肝损伤时,应定期监测患者的肝功能,长期用药者每月一次;如果肝酶水平升高幅度<3倍正常值上限,无需调整托珠单抗剂量或可考虑调整甲氨蝶呤剂量;如升高幅度>3~5倍正常值上限,需停药 4周;如升高幅度>5倍正常值上限,则需永久停药。
为避免患者出现高胆固醇血症,用药前应检测患者的血脂基线水平,用药后定期监测其血脂变化,如有异常需根据高胆固醇血症相关指南,启动他汀类药物治疗。当患者出现嗜中性粒细胞减少的情况,应定期监测,如嗜中性粒细胞绝对计数>1×(10³)³/L,则无需干预;若嗜中性粒细胞绝对计数为(0. 5~1)×(10³)³/L,则需停药 4 周;若绝对计数< 0. 5×(10³)³/L,则需永久停药。另外,在前6次托珠单抗(tocilizumab)的输注过程中应密切监测患者的过敏指征,若患者因过敏反应不能完成本次输注,切勿反复尝试再次给药。
参考资料: FDA说明书更新于2025年8月8日,说明书网址:https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=125276
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
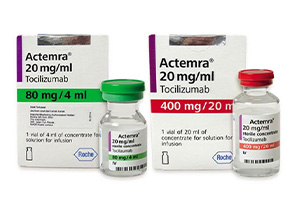
药品信息

- 托珠单抗的适应症托珠单抗是一种靶向IL-6受体的单克隆抗体,通过抑制IL-6介导的炎症反应,在多...[ 详情 ]推荐指数:7462025-08-06 10:48:33
- 托珠单抗的用药指南托珠单抗(Tocilizumab)是一种靶向IL-6受体的单克隆抗体,广泛应用于...[ 详情 ]推荐指数:8552025-08-06 10:48:43
- 托珠单抗的副作用与注意事项托珠单抗是一种靶向IL-6受体的生物制剂,在治疗多种免疫相关疾病中显示出显著疗效...[ 详情 ]推荐指数:9622025-08-06 10:48:55
- 托珠单抗的副作用如何缓解托珠单抗是一种靶向IL-6受体的生物制剂,广泛用于治疗类风湿性关节炎、细胞因子释...[ 详情 ]推荐指数:6522025-08-05 16:28
- 托珠单抗的国内价格是多少托珠单抗是一种重要的生物制剂,广泛应用于类风湿性关节炎、巨细胞动脉炎等多种疾病的...[ 详情 ]推荐指数:14702025-08-05 16:16
- 罗氏抗(tocilizumab)治疗类风湿关节炎的作用功效,用法用量,副作用,注意事项及疗效?关于罗氏抗(tocilizumab)类风湿性关节炎(RA)是一种全身性炎症性疾病...[ 详情 ]推荐指数:12422024-12-05 14:27:17
- 托珠单抗注射液的注射方法以及注意事项?注射方法托珠单抗皮下制剂采用一次性使用的预充式注射器加带针头安全装置给药。使用托...[ 详情 ]推荐指数:15372024-12-05 14:27:17
- 托珠单抗治疗新冠的作用机制以及效果?新型冠状病毒感染新型冠状病毒是一种已知会引起呼吸道疾病的病毒,自2002年以来已...[ 详情 ]推荐指数:12152024-12-05 14:27:17
- 罗氏抗(tocilizumab)联合甲氨蝶呤治疗类风湿关节炎要打多久?罗氏抗(tocilizumab)联合甲氨蝶呤治疗类风湿关节炎通常要打2个月左右。...[ 详情 ]已帮助847人2023-12-15 10:07
- 肺炎患者可以用罗氏抗(tocilizumab)吗?肺炎患者不可以使用罗氏抗(tocilizumab)。罗氏抗(tocilizuma...[ 详情 ]已帮助853人2023-12-15 10:07
- 罗氏抗(tocilizumab)会引起肝损伤吗?罗氏抗(tocilizumab)会引起肝损伤。罗氏抗(tocilizumab)具...[ 详情 ]已帮助845人2023-12-15 10:07
- 罗氏抗(tocilizumab)最大的副作用是什么?罗氏抗(tocilizumab)最大的副作用是严重感染。1、全身感染:据报道,接...[ 详情 ]已帮助855人2023-12-15 10:07
- 托珠单抗是免疫抑制剂吗?托珠单抗是一种生物免疫抑制剂,2013年在中国获批用于治疗中到重度活动性类风湿关...[ 详情 ]已帮助1595人2023-11-09 02:57:02
- 托珠单抗治疗类风湿关节炎打多久?治疗类风湿性关节炎时,托珠单抗tocilizumab可单独使用或与氨甲喋呤或其它...[ 详情 ]已帮助1580人2023-11-04 13:20:38
- 托珠单抗可以治疗血管炎吗?托珠单抗(TCZ)治疗大血管炎有效,包括巨细胞动脉炎(GCA)。既往,有2期试验...[ 详情 ]已帮助1526人2023-11-13 10:09:54
- 托珠单抗会使白介素6升高吗?有关研究显示,类风湿性关节炎患者的白介素-6水平升高,而托珠单抗(罗氏抗)正是被...[ 详情 ]已帮助2488人2023-11-16 09:45:50
- PM8002联合紫杉醇对比化疗二线治疗小细胞肺癌[适 应 症]小细胞肺癌[试验分期]Ⅱ期
- ES102联合特瑞普利单抗治疗晚期非小细胞肺癌[适 应 症]非小细胞肺癌[试验分期]Ⅱ期
- 比较Sigvotatug Vedotin与多西他赛治疗既往经治的非小细胞肺癌的研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- QL2107或Keytruda®联合化疗治疗转移性非鳞状非小细胞肺癌的临床研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- LM-299注射液单药或联合其它抗肿瘤药物治疗晚期实体瘤[适 应 症]实体瘤[试验分期]Ⅰ期
- SH-1028片对比安慰剂用于非小细胞肺癌辅助治疗[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
做您身边的贴心健康咨询管家

了解医药信息 关注临床动态
- 1厄达替尼(Erdafitinib)的功效与作用已帮助38人2026-04-07 17:55
- 2艾加莫德(Vyvgart)用药指南已帮助29人2026-04-07 17:55
- 3卡那单抗(Ilaris)在哪里可以买到?已帮助32人2026-04-07 17:55
- 4阿那格雷(Anagrelide)的价格是多少?已帮助28人2026-04-07 17:53
- 5苯巴那酯(森巴考特)国内价格是多少?已帮助31人2026-04-07 17:44
- 6苯巴那酯(Cenobamate)多少钱一盒?已帮助36人2026-04-07 17:22
- 7氧氟沙星耳科用液(Tarivid)的用药注意事项已帮助39人2026-04-07 16:33:38
- 8氧氟沙星耳科用液(Tarivid)的功效与作用已帮助35人2026-04-07 16:33:28
- 9布瑞索卡替(Brensocatib)的注意事项和药物相互作用已帮助39人2026-04-07 17:20:08
- 10布瑞索卡替(Brensocatib)是治疗什么疾病的已帮助35人2026-04-07 15:50
- 11FDA批准礼来公司塞尔帕替尼(Retevmo),为首个且唯一用于RET基因融合阳性晚期或转移性实体瘤成人患者的RET抑制剂,不限肿瘤类型已帮助35人2026-04-07 15:19
- 12美国食品药品监督管理局(FDA)加速批准塞尔帕替尼(Retevmo)用于两岁及以上RET突变型转移性甲状腺癌或实体瘤儿科患者已帮助42人2026-04-07 15:18
 硫酸氢氯吡格雷(Plavix)硫酸氢氯吡格雷需联合阿司匹林用于急性冠脉综合征(...[ 详情 ]
硫酸氢氯吡格雷(Plavix)硫酸氢氯吡格雷需联合阿司匹林用于急性冠脉综合征(...[ 详情 ] 卡巴胆碱和酒石酸溴莫尼定眼用溶液(Yuvezzi)Yuvezzi适用于成人老视的治疗。老视是一种与...[ 详情 ]
卡巴胆碱和酒石酸溴莫尼定眼用溶液(Yuvezzi)Yuvezzi适用于成人老视的治疗。老视是一种与...[ 详情 ] 欧维婷(Ovestin)欧维婷适用于绝经后女性(距末次自然月经至少12个...[ 详情 ]
欧维婷(Ovestin)欧维婷适用于绝经后女性(距末次自然月经至少12个...[ 详情 ] 欧龙马口服滴剂(Sinupret Tropfen)适用于急性及慢性鼻窦炎的辅助治疗,尤其适用于存在...[ 详情 ]
欧龙马口服滴剂(Sinupret Tropfen)适用于急性及慢性鼻窦炎的辅助治疗,尤其适用于存在...[ 详情 ]