venetoclax需要注意什么?

venetoclax目前已被美国FDA批准用于治疗曾服用多种药物且复发难治的染色体17p 缺失型慢性淋巴细胞白血病,也是美国FDA批准的首个B细胞淋巴瘤因子-2(B-cell lymphoma 2,BCL-2)小分子抑制剂类药物。许多患者不了解维奈托克的注意事项,导致疗效没有达到预期,故而,患者应了解维奈托克注意事项并规避,才能达到预期效果。
venetoclax注意事项,剂量调整的指导原则 中断服药剂量及重新开始服药的剂量调整分别为:400 mg·d-1改为300 mg·d-1;300 mg·d-1改为200 mg·d-1;200 mg·d-1改为100 mg·d-1;100 mg·d-1改为50 mg·d-1;50 mg·d-1改为20 mg·d-1;20 mg·d-1改为10 mg·d-1。在剂量递增期,增加剂量需减小剂量为期1周;漏服剂量的处置 在8 h内漏服一剂,应尽可能立即补服,并恢复正常每日的服药时间表。若超过8 h,不能补服,按正常的时间表服下一天的剂量。患者服药后发生呕吐,当日不另外补服,按正常的时间表服下一天的剂量;Venclexta的常见不良反应有:(≥20%)为中性粒细胞减少,腹泻,恶心,贫血,上呼吸道感染,血小板减少,和疲乏。与CYP3A和P-gp抑制药同服时的剂量调整 开始服药及剂量递增期,应避免与强CYP3A抑制药同服,会增加venetoclax的接触量,发生TLS风险,已完成剂量递增期服药后,必须与强CYP3A抑制药同服,venetoclax的日剂量至少减75%;避免与中度CYP3A抑制药或P-gp抑制药同时服用,可考虑其他治疗方法,若必须同服,venetoclax的日剂量应减50%,并严密监控毒性反应。
参考资料: FDA说明书更新于2022年6月15日,FDA说明书网址:https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=208573
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
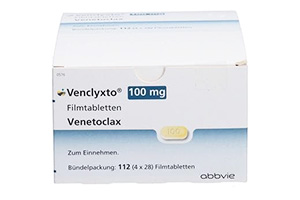
药品信息

- 维奈克拉片(Venetoclax)的作用功效,如何用药适应症1、CLL或SLL维奈克拉片用于治疗慢性淋巴细胞白血病(CLL)和小淋巴细...[ 详情 ]推荐指数:1052026-03-12 17:49:01
- 维奈克拉片(Venetoclax)纳入医保了吗?维奈克拉片(Venetoclax)是一种突破性的靶向治疗药物,已被纳入国家医保目...[ 详情 ]推荐指数:7402025-10-17 11:27:34
- 维奈克拉片的副作用和注意事项维奈克拉片是全球首个靶向BCL-2蛋白的小分子抑制剂,在慢性淋巴细胞白血病和急性...[ 详情 ]推荐指数:6882025-07-09 17:45
- 维奈克拉片的副作用如何缓解维奈克拉片是全球首个靶向BCL-2蛋白的小分子抑制剂,在血液系统恶性肿瘤治疗中展...[ 详情 ]推荐指数:7382025-07-09 17:30
- 维奈克拉片的用药指南维奈克拉片是全球首个靶向BCL-2蛋白的小分子抑制剂,在慢性淋巴细胞白血病和急性...[ 详情 ]推荐指数:6762025-07-09 17:24
- 维奈克拉片的功效与作用维奈克拉片是一种靶向BCL-2蛋白的小分子抑制剂,由美国艾伯维公司研发,主要用于...[ 详情 ]推荐指数:7102025-07-09 17:18
- 维奈克拉一个疗程几盒?多少钱?维奈克拉是一种用于治疗慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL),...[ 详情 ]推荐指数:7012025-07-04 11:29:00
- 维奈克拉一次能囤几盒?多少钱?维奈克拉在购买数量、价格以及特殊人群用药方面都有其特定的要求和注意事项,了解这些...[ 详情 ]推荐指数:5602025-06-09 17:55
- 维奈克拉能用医保报销吗?维奈克拉已经纳入医保目录,可以进行医保报销。根据搜索结果,维奈克拉作为“乙类”药...[ 详情 ]已帮助889人2024-05-29 11:37
- 维奈克拉用后出现感染怎么处理?维奈克拉用后出现感染,需要评估感染的严重程度和部位。维奈克拉使用后出现的感染可能...[ 详情 ]已帮助846人2024-05-29 11:36
- 的维奈克拉价格是多少钱一盒2024年?老挝仿制的维奈克拉2024年的价格大约是1960$-5500$一盒。老挝仿制的维...[ 详情 ]已帮助907人2025-08-18 13:20:39
- 维奈克拉价格是多少钱一盒2025年?孟加拉的维奈克拉2024年的价格大约是1750$-2300$。孟加拉的维奈克拉属...[ 详情 ]已帮助884人2025-08-15 17:15:53
- 吃完维奈克拉后便秘怎么办?吃完维奈克拉后便秘主要是药物不良反应导致,可通过增加膳食纤维摄入、多喝水、适量运...[ 详情 ]已帮助864人2024-03-07 09:12
- 维奈克拉吃多长时间可以停药?维奈克拉吃多长时间可以停药临床上没有统一的标准,可能是几个月也有可能是数年,需要...[ 详情 ]已帮助1140人2024-03-07 09:03
- 维奈克拉2024年在哪里能买到?关于2024年维奈克拉的购买渠道,以下是一些可能的选择:1、医院药房:维奈克拉是...[ 详情 ]已帮助883人2024-02-29 11:24
- 维奈克拉能治好白血病吗?维奈克拉通常可以治疗白血病,可以延长生存期,在治疗白血病方面取得了一定的效果,但...[ 详情 ]已帮助894人2024-02-29 11:22
- PM8002联合紫杉醇对比化疗二线治疗小细胞肺癌[适 应 症]小细胞肺癌[试验分期]Ⅱ期
- ES102联合特瑞普利单抗治疗晚期非小细胞肺癌[适 应 症]非小细胞肺癌[试验分期]Ⅱ期
- 比较Sigvotatug Vedotin与多西他赛治疗既往经治的非小细胞肺癌的研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- QL2107或Keytruda®联合化疗治疗转移性非鳞状非小细胞肺癌的临床研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- LM-299注射液单药或联合其它抗肿瘤药物治疗晚期实体瘤[适 应 症]实体瘤[试验分期]Ⅰ期
- SH-1028片对比安慰剂用于非小细胞肺癌辅助治疗[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
做您身边的贴心健康咨询管家

了解医药信息 关注临床动态
- 1氟维司群(Fulvestrant)的作用功效、用药指南已帮助71人2026-04-03 17:45
- 2伊布替尼(Imbruvica)的适应症、副作用已帮助73人2026-04-03 17:45
- 3卡替拉韦(Cabotegravir)的作用功效已帮助116人2026-04-03 17:45
- 4苯巴那酯(Cenobamate)的功效与作用已帮助69人2026-04-03 17:43
- 5沙芬酰胺(Safinamide)说明书:功效与作用、副作用已帮助103人2026-04-03 17:31
- 6沙芬酰胺(Safinamide)的适应症和疗效已帮助78人2026-04-03 17:20
- 7沙芬酰胺(Safinamide)国内能买到吗?在哪能买到?已帮助80人2026-04-03 17:04
- 8沙芬酰胺(Safinamide)在哪里可以买到?已帮助81人2026-04-03 16:56
- 9布瑞索卡替(Brensocatib)国内能买到吗?在哪能买到?已帮助69人2026-04-03 16:42
- 10布瑞索卡替(Brensocatib)国内价格是多少已帮助76人2026-04-03 16:27
- 11布瑞索卡替(Brensocatib)的副作用如何缓解已帮助74人2026-04-03 16:01:58
- 12布瑞索卡替(Brensocatib)的用药注意事项已帮助84人2026-04-03 15:45:05
 卡巴胆碱和酒石酸溴莫尼定眼用溶液(Yuvezzi)Yuvezzi适用于成人老视的治疗。老视是一种与...[ 详情 ]
卡巴胆碱和酒石酸溴莫尼定眼用溶液(Yuvezzi)Yuvezzi适用于成人老视的治疗。老视是一种与...[ 详情 ] 欧维婷(Ovestin)欧维婷适用于绝经后女性(距末次自然月经至少12个...[ 详情 ]
欧维婷(Ovestin)欧维婷适用于绝经后女性(距末次自然月经至少12个...[ 详情 ] 欧龙马口服滴剂(Sinupret Tropfen)适用于急性及慢性鼻窦炎的辅助治疗,尤其适用于存在...[ 详情 ]
欧龙马口服滴剂(Sinupret Tropfen)适用于急性及慢性鼻窦炎的辅助治疗,尤其适用于存在...[ 详情 ] 布瑞索卡替(Brensocatib)布瑞索卡替适用于治疗12岁及以上成人和儿童患者的...[ 详情 ]
布瑞索卡替(Brensocatib)布瑞索卡替适用于治疗12岁及以上成人和儿童患者的...[ 详情 ]