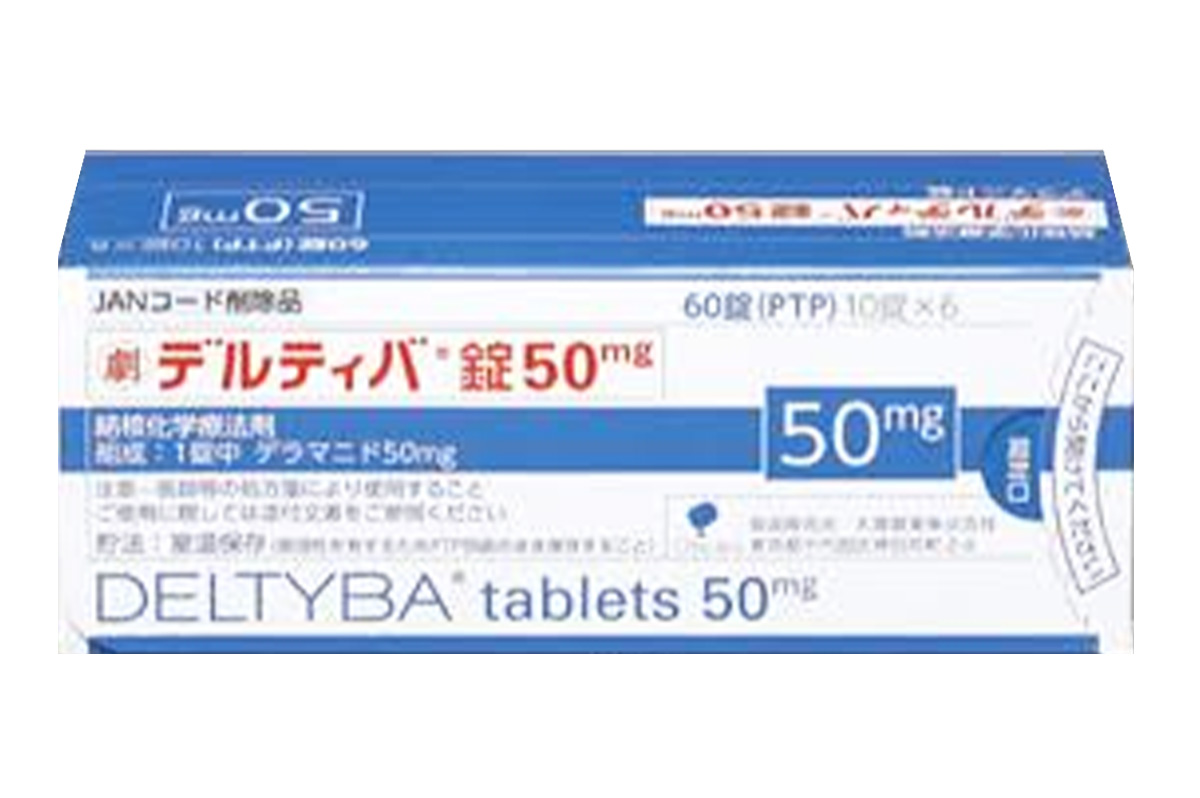



德拉马尼(Delamanid)
图片来源: 图片来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供参考。
德拉马尼由日本大冢制药有限公司(Otsuka Pharmaceutical Co.,Ltd.)研发生产,于2014年由欧洲药品管理局(EMA)有条件地批准上市,建议用于成人MDR-TB患者因耐药或耐受性原因无法组成有效方案时。
德拉马尼在国内的上市时间为2023年9月,且已纳入我国医保药品报销名录,限用于耐多药结核患者。

德拉马尼主要通过抑制MTB细胞壁甲氧基分枝菌酸及酮基分枝菌酸的合成来发挥杀菌作用。它对MTB敏感菌株、多重耐药菌株、休眠期菌株及胞内菌株均具有较强杀菌作用,且与其他抗结核药物无交叉耐药性。
药品称呼
通用名称:Delamanid、德拉马尼
商品名称:Deltyba、德尔巴
适应靶点
结核分枝杆菌。
适应症和适应人群
对德拉马尼敏感的多药耐药肺结核成年患者。
规格和性状
规格
50mg*60片/盒。
性状
黄褐色圆形片剂。
主要成分
活性成分:德拉马尼。
用法用量
德拉马尼成人患者每日口服两次,每次100毫克,每12小时一次;6-11岁儿童每日口服两次,每次50毫克;12-17岁青少年每日口服两次,每次100毫克。
关于德拉马尼的具体用法用量内容,您可以阅读完整德拉马尼用药指南信息。推荐文章:德拉马尼(Delamanid)的用法用量。
不良反应
重大副作用
QT间期延长(发生率≥5%),可能导致心律失常风险增加,临床需重点监测。
用药期间需密切观察患者反应,一旦出现异常,应立即采取停药等相应处置措施。推荐文章:德拉马尼(Delamanid)的副作用。
注意事项
本药仅限有结核治疗经验的医生,在参与RAP计划的机构为注册患者开具,以确保合理用药、防止耐药。
因可能引起QT间期延长,用药前后需定期检查心电图、电解质(钾、镁、钙)和血清白蛋白,评估风险后再决定是否继续使用。
联合抗结核治疗时可能出现病情反跳(如原有症状加重或新发症状),应根据药敏试验结果判断是否继续用药。
有QT延长病史、心动过缓、电解质紊乱、心脏病或低白蛋白血症者,QT延长风险更高,应谨慎评估后使用。
服药时须将药片从PTP板上取出,切勿连同包装吞服,以免锐角刺伤食道,引发严重并发症。
药品具吸湿性,应密封保存于原PTP包装中,防潮以保证疗效。
特殊人群用药
【孕妇】禁用。动物实验(兔)显示,给予德拉马尼后早期吸收胚数量增加;动物实验(大鼠)显示,给予其主要代谢物后,胎儿外形异常、内脏及骨骼变异的发生率升高,且德拉马尼可通过胎盘屏障,故孕妇或有妊娠可能的女性严禁使用。
【哺乳期女性】不建议哺乳。动物实验(大鼠)显示,德拉马尼可转移至乳汁中,为避免对乳儿造成潜在风险,哺乳期女性使用德拉马尼期间应暂停哺乳。
【儿童使用】18岁以下患者的临床安全性和有效性尚未确立,未开展相关临床试验。国外有儿童使用德拉马尼后出现幻觉的报告,故不推荐18岁以下患者使用。
【老年人使用】老年人因生理功能(如肝肾功能、代谢能力)呈生理性减退,使用德拉马尼时需密切观察患者状态,谨慎给药,必要时根据患者具体情况调整用药方案。
【肝功能损害】肝功能损害患者使用德拉马尼时,药物原形及代谢物的血浆浓度可能升高,从而增加QT延长等副作用的发生风险,需严格评估风险与获益,谨慎用药,并加强相关指标监测。
禁忌症
对德拉马尼或本药制剂中任何一种辅料过敏者。
孕妇或有妊娠可能的女性。
药物相互作用
联用QT延长药物的风险
与已知可引起QT延长的药物联用时,可能产生相加性QT延长效应,增加心律失常风险,需谨慎权衡利弊。此类药物包括喹诺酮类抗菌药(如盐酸莫西沙星、左氧氟沙星水合物等)、ⅠA类抗心律失常药(如硫酸奎尼丁水合物、盐酸普鲁卡因胺等)、Ⅲ类抗心律失常药(如盐酸胺碘酮、盐酸索他洛尔等),以及舒必利、盐酸丙咪嗪、匹莫齐特、氟哌啶醇、红霉素、索利那新琥珀酸盐、富马酸贝达喹啉等。
联用致低血钾药物的风险
与可能引发低血钾症的药物联用时,会增加电解质紊乱相关的QT延长风险,需密切监测电解质水平。此类药物包括氨基糖苷类抗菌药(如硫酸恩维霉素、硫酸卡那霉素等)、利尿剂(如呋塞米、三氯噻嗪等)及两性霉素B等。
与抗结核药物的相互作用
与抗结核药物联用时,本药对利福平、异烟肼、吡嗪酰胺的血药浓度无显著影响,但会使乙胺丁醇的Cmax升高27%、AUC升高23%;而利福平、异烟肼、吡嗪酰胺、乙胺丁醇联合使用时,会使本药的Cmax和AUC均降低45%。
与抗HIV药物的相互作用
与抗HIV药物联用时,本药对替诺福韦、洛匹那韦/利托那韦、依法韦仑的血药浓度无显著影响;替诺福韦、依法韦仑对本药的血药浓度无显著影响,但洛匹那韦/利托那韦会使本药的Cmax升高18%、AUC升高22%。
药物过量
症状
过量给药可能导致QT间期延长,增加心律失常风险。
处置
一旦发生药物过量,需立即实施心电图检查,并对患者进行密切监护,根据患者的临床症状及检查结果,采取相应的支持治疗和对症处理措施。
药代动力学
吸收:本药的吸收受饮食影响显著,空腹口服时的吸收程度显著低于餐后,高脂肪饮食可显著增加药物的吸收程度。
分布:德拉马尼及其代谢物DM-6705的人血清蛋白结合率均≥99.5%(体外平衡透析法测定)。
代谢:德拉马尼主要在血浆中经白蛋白代谢,同时可被细胞色素P4503A4(CYP3A4)少量代谢;其代谢物DM-6705可经CYP3A4、CYP1A1、CYP2D6及CYP2E1代谢。
排泄:健康成人餐后单回口服14C-德拉马尼100mg后,89%的放射能经粪便排泄,3%经尿液排泄。
贮存方法
室温保存,密封于原PTP包装中,避免吸潮。
研发企业
日本大冢
参考资料:日本药监局更新于2023年11月13日,说明书网址:https://www.info.pmda.go.jp/go/pack/6222006F1029_1_11/?view=frame&style=XML&lang=ja
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
- 德拉马尼多少钱一盒?据了解,德拉马尼规格为50mg*48粒,参考价格约为10950$~12000$之...[ 详情 ]推荐指数:26492025-01-21 15:34:11
- 德拉马尼(Delamanid)的功效与作用及副作用?德拉马尼(Delamanid)是第一种双环硝基咪唑,被批准用于耐多药结核病治疗。...[ 详情 ]推荐指数:16112025-01-21 07:27:10
- 德拉马尼治疗耐多药肺结核效果显著吗?德拉马尼治疗耐多药肺结核效果显著。德拉马尼作为抗结核新药对耐多药和广泛耐药结核病...[ 详情 ]推荐指数:13162025-01-21 15:24:39
- 德拉马尼片肺结核的治愈率是多少德拉马尼Ⅱ期临床试验主要关注痰培养结果转阴率,结果发现MDR-TB(肺部多重耐药...[ 详情 ]推荐指数:13782025-01-21 18:07:27
- 德拉马尼片是新特药吗?新发结核病患者中约55.8万人为耐利福平结核病(RR-TB),而在RR-TB患者...[ 详情 ]推荐指数:15932025-01-21 11:02:06
- 德拉马尼片一个月药费多少?耐多药结核病(MDR-TB)是由至少对异烟肼和利福平这两种一线用于TB药物耐药的...[ 详情 ]推荐指数:18842025-01-21 09:50:11
- 抗结核新药德拉马尼的功效与作用?德拉马尼的功效与作用德拉马尼/Delamanid是一种新的分枝菌酸生物合成抑制剂...[ 详情 ]推荐指数:21202025-01-21 09:21:35
- 德拉马尼的剂量与用法是什么?德拉马尼(Delamanid)是一种硝基二氢咪唑衍生物,对结核分枝杆菌的药物敏感...[ 详情 ]推荐指数:15582025-01-21 04:45:00
- 德拉马尼能与洛匹那韦/利托那韦一起使用吗?德拉马尼能与洛匹那韦/利托那韦最好不要一起使用。德拉马尼与CYP3A强抑制剂(如...[ 详情 ]已帮助972人2024-02-08 15:18
- 哪些人不能使用德拉马尼?1、过敏史:对德拉马尼的活性成分或任何辅料有过敏史的患者禁用。过敏反应可能包括皮...[ 详情 ]已帮助973人2024-02-08 15:18
- 德拉马尼适用于全年龄的人吗?德拉马尼(Delamanid)是一种用于结核病治疗的药物,目前仅获准用于成年人和...[ 详情 ]已帮助997人2024-02-08 15:18
- 德拉马尼在国内医院能买到吗?德拉马尼在国内医院就可以购买到。目前,德拉马尼已经在中国上市,并且进入国家医保当...[ 详情 ]已帮助966人2024-02-08 15:04:37
- 德拉马尼片什么时候上市的?德拉马尼片于2012年在美国获批上市,2014年日本等地区获批上市,2018年在...[ 详情 ]已帮助1559人2023-11-16 07:40:19
- 德拉马尼(Delamanid)的禁忌症是什么?德拉马尼(Delamanid)的禁忌症主要包括以下几点。1、对德拉马尼或其任何成...[ 详情 ]已帮助1608人2023-11-16 07:40:43
- 德拉马尼(Delamanid)用药过量怎么办?德拉马尼(Delamanid)用药过量应立即采取措施清除胃肠道中的德拉马尼,并根...[ 详情 ]已帮助1466人2023-11-15 17:09:07
- 德拉马尼适用于哪些人群?德拉马尼适用于18岁以上成人肺部耐多药结核病(MDR-TB),因为耐药性或耐受性...[ 详情 ]已帮助1521人2023-11-04 11:35:48
- PM8002联合紫杉醇对比化疗二线治疗小细胞肺癌[适 应 症]小细胞肺癌[试验分期]Ⅱ期
- ES102联合特瑞普利单抗治疗晚期非小细胞肺癌[适 应 症]非小细胞肺癌[试验分期]Ⅱ期
- 比较Sigvotatug Vedotin与多西他赛治疗既往经治的非小细胞肺癌的研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- QL2107或Keytruda®联合化疗治疗转移性非鳞状非小细胞肺癌的临床研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- LM-299注射液单药或联合其它抗肿瘤药物治疗晚期实体瘤[适 应 症]实体瘤[试验分期]Ⅰ期
- SH-1028片对比安慰剂用于非小细胞肺癌辅助治疗[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
做您身边的贴心健康咨询管家

了解医药信息 关注临床动态
- 1普乐沙福(Plerixafor)的适应症与注意事项已帮助51人2026-05-19 17:52:30
- 2阿比特龙(Abiraterone)的用药指南与不良反应已帮助46人2026-05-19 17:43
- 3尼拉帕尼(Niraparib)的适应症、副作用已帮助48人2026-05-19 17:43
- 4那他珠单抗国内哪里能买到?已帮助41人2026-05-19 17:36
- 5那他珠单抗国内价格是多少?已帮助38人2026-05-19 17:36
- 6那他珠单抗价格是多少?已帮助45人2026-05-19 17:27
- 7Strensiq价格多少钱一盒?已帮助48人2026-05-19 17:16
- 8阿福他酶α多少钱一盒?已帮助45人2026-05-19 17:02
- 9阿福他酶α国内哪里能买到?已帮助53人2026-05-19 16:43
- 10宗格替尼国内能买到吗?已帮助53人2026-05-19 16:31
- 11盐酸环苯扎林舌下含服片的价格是多少?已帮助45人2026-05-19 15:47
- 12盐酸环苯扎林舌下含服片怎么购买?已帮助41人2026-05-19 15:47
 盐酸可乐定(Javadin)用于成人高血压患者的血压控制,通过降低血压,减少...[ 详情 ]
盐酸可乐定(Javadin)用于成人高血压患者的血压控制,通过降低血压,减少...[ 详情 ] 莱达西贝普(lerodalcibep-liga)作为饮食控制与运动干预的辅助治疗药物,用于成人高...[ 详情 ]
莱达西贝普(lerodalcibep-liga)作为饮食控制与运动干预的辅助治疗药物,用于成人高...[ 详情 ] Nuzolvence(Zoliflodacin)适用于12岁及以上、体重≥35kg的成人及青少年...[ 详情 ]
Nuzolvence(Zoliflodacin)适用于12岁及以上、体重≥35kg的成人及青少年...[ 详情 ] 依特立生(Eteplirsen)适用于经基因检测确诊、DMD基因突变可实现51号...[ 详情 ]
依特立生(Eteplirsen)适用于经基因检测确诊、DMD基因突变可实现51号...[ 详情 ]



 医伴旅服务热线:
医伴旅服务热线:
































