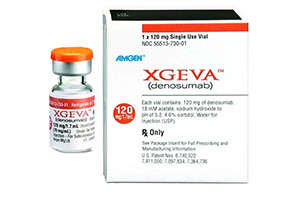
美国安进狄诺塞麦在中国上市了吗?

骨巨细胞瘤(Giantcelltumorofbone,GCTB)是一种良性侵袭性(交界)骨肿瘤。由Cooper和Travers首先报道,在美国,GCTB约占原发骨肿瘤的5%,在中国和印度更为常见,约占所有原发骨肿瘤的20%。GCTB好发年龄为20-40岁,女性多见。过去,对于GCTB的全身治疗包括二膦酸盐,化疗,干扰素-α,达沙替尼和舒尼替尼。多数循证医学证据等级不高,也非普遍应用的标准疗法。近年来,狄诺塞麦作为一种新的治疗方式引起广泛关注。
作为全球最大生物制药企业之一的“安进公司”(Amgen),贵为全球生物医药产业领头羊,拥有极强的研发能力和产品优势,坚持在疾病治疗的生物技术领域内发展,主要涉足的领域有人类基因组,癌症,神经科学和小分子化学等。狄诺塞麦最初由Amgen公司研发用于治疗骨质疏松,2004年一项I期临床试验初步验证狄诺塞麦对于抑制骨吸收的疗效和安全性,之后于2009年一项包括7868名骨质疏松的女性患者的随机对照试验(FREEDOMTrial)证实,狄诺塞麦组相比安慰剂对照组可显著减少骨折风险32%(p<0.001)。同时,Smith等(DenosumabHALTProstateCancerStudyGroup)报道了包含1468名经过去势治疗的未转移前列腺癌患者的随机对照试验,狄诺塞麦治疗后可增加骨密度及减少新发椎体骨折风险。
2019年05月23日,中国国家药品监督管理局宣布有条件批准(安加维)狄诺塞麦注射液(英文名:Denosumab Injection)进口注册申请。狄诺塞麦将用于骨巨细胞瘤不可手术切除或者手术切除可能导致严重功能障碍的成人和骨骼发育成熟的青少年患者治疗。
相关热文推荐:安进狄诺塞麦适应症/newsDetail/93100.html
参考资料: FDA说明书更新于2025年5月30日,说明书网址:https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=125320
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
- 地舒单抗多少钱一支地舒单抗是一种用于治疗骨质疏松症、实体肿瘤骨转移的生物制剂,由美国安进公司生产,...[ 详情 ]推荐指数:10862025-05-13 13:23
- 地舒单抗的功效和副作用地舒单抗是一种广泛应用于骨质疏松症和骨转移治疗的生物制剂,通过抑制破骨细胞活性减...[ 详情 ]推荐指数:11802025-05-15 09:59:02
- 地舒单抗最新公布价格表导读:地舒单抗是一种创新性的生物制剂,正逐步成为骨科及肿瘤治疗领域的重要药物,可...[ 详情 ]推荐指数:25162025-03-04 09:12:11
- 地舒单抗一次能囤几盒?多少钱?导读:2020年11月地舒单抗的新适应症获批,用于预防实体瘤骨转移和多发性骨髓瘤...[ 详情 ]推荐指数:8232025-03-04 14:40:43
- 地舒单抗在中国上市了吗?好购买吗?导读:地舒单抗是一种全人源单克隆抗体,通过高亲和力与RANKL结合,抑制RANK...[ 详情 ]推荐指数:8602025-03-04 15:16:10
- 地舒单抗有几种规格?多少钱?导读:地舒单抗在临床用于骨质疏松、骨巨细胞瘤、多发性骨髓瘤和实体肿瘤骨转移的治疗...[ 详情 ]推荐指数:22392025-03-04 14:12:31
- 地舒单抗多少钱一盒?在哪里购买?导读:地舒单抗于2019年5月21日获批在国内上市,其上市为国内骨质疏松的治疗提...[ 详情 ]推荐指数:15292025-03-04 14:08:15
- 地舒单抗费用大概多少导读:地舒单抗主要用于骨科肿瘤疾病的治疗,如实体肿瘤骨转移、多发性骨髓瘤和骨巨细...[ 详情 ]推荐指数:11642025-03-04 13:29:00
- 地舒单抗停用了对人体有什么影响?地舒单抗停用了对人体的影响主要包括骨密度下降、骨折风险增加、治疗效果消失等。1、...[ 详情 ]已帮助1235人2024-03-13 14:08
- 打完地舒单抗能吃骨疏康胶囊吗?打完地舒单抗通常能吃骨疏康胶囊,但是需要谨遵医嘱。地舒单抗通过抑制RANKL来减...[ 详情 ]已帮助1039人2024-03-13 13:59
- 地舒单抗一次可以注射两针吗?地舒单抗一次不可以注射两针。地舒单抗一支的规格是120mg,推荐剂量是120mg...[ 详情 ]已帮助1021人2024-03-13 09:20:05
- 打地舒单抗会出现髋关节疼吗?打地舒单抗可能会出现髋关节疼。地舒单抗的常见副作用包括低钙血症、皮肤反应、疲劳、...[ 详情 ]已帮助908人2024-03-13 11:54
- 地舒单抗买回来怎么保存?地舒单抗的正确保存方法如下:1、保存温度:将地舒单抗保存在原始温度为2°C至8°...[ 详情 ]已帮助1122人2024-02-18 13:36
- 地舒单抗的副作用多久能消失?地舒单抗副作用消失的时间因人而异,通常大多数副作用可在停药后消失,但有些副作用后...[ 详情 ]已帮助1164人2024-02-18 13:36
- 打了地舒单抗后能拔牙吗?打了地舒单抗后一般不能拔牙。地舒单抗是一种RANK配体(RANKL)抑制剂,能结...[ 详情 ]已帮助1172人2024-02-18 13:36
- 打地舒单抗可以吃蜂王浆吗?打地舒单抗可以吃蜂王浆,但具体用法用量应咨询医生。地舒单抗是一种人类单克隆抗体,...[ 详情 ]已帮助836人2024-02-18 13:36
- PM8002联合紫杉醇对比化疗二线治疗小细胞肺癌[适 应 症]小细胞肺癌[试验分期]Ⅱ期
- ES102联合特瑞普利单抗治疗晚期非小细胞肺癌[适 应 症]非小细胞肺癌[试验分期]Ⅱ期
- 比较Sigvotatug Vedotin与多西他赛治疗既往经治的非小细胞肺癌的研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- QL2107或Keytruda®联合化疗治疗转移性非鳞状非小细胞肺癌的临床研究[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- LM-299注射液单药或联合其它抗肿瘤药物治疗晚期实体瘤[适 应 症]实体瘤[试验分期]Ⅰ期
- SH-1028片对比安慰剂用于非小细胞肺癌辅助治疗[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
做您身边的贴心健康咨询管家

了解医药信息 关注临床动态
- 1左甲状腺素钠片(Euthyrox)的适应症及用法用量已帮助3人2026-03-19 17:51
- 2佩米替尼(pemigatinib)的适应症和用法用量已帮助4人2026-03-19 17:45
- 3奥拉帕利(Olaparib)用药指南已帮助3人2026-03-19 17:41
- 4Yartemlea(Narsoplimab-wuug)的用法用量已帮助3人2026-03-19 17:41
- 5Yartemlea(Narsoplimab-wuug)怎么购买已帮助3人2026-03-19 17:41
- 6Yartemlea(Narsoplimab-wuug)的副作用如何缓解已帮助3人2026-03-19 17:32
- 7Yartemlea(Narsoplimab-wuug)的用药注意事项已帮助5人2026-03-19 17:10
- 8Yartemlea(Narsoplimab-wuug)的功效与作用已帮助6人2026-03-19 16:40
- 9舒泽曲近片(Journavx)国内能买到吗?在哪能买到?已帮助6人2026-03-19 16:32
- 10舒泽曲近片(Journavx)的用药指南已帮助10人2026-03-19 17:57:44
- 11舒泽曲近片(Journavx)的用法用量已帮助6人2026-03-19 15:48
- 12舒泽曲近片(Journavx)怎么购买已帮助6人2026-03-19 15:35
 卡比多巴左旋多巴缓释胶囊(Crexont)适用于成人患者以下病症的治疗:帕金森病、脑炎后帕...[ 详情 ]
卡比多巴左旋多巴缓释胶囊(Crexont)适用于成人患者以下病症的治疗:帕金森病、脑炎后帕...[ 详情 ] 苯磺酸米洛沙巴林(Tarlige)主要用于成人患者的神经病理性疼痛。[ 详情 ]
苯磺酸米洛沙巴林(Tarlige)主要用于成人患者的神经病理性疼痛。[ 详情 ] 阿托伐醌(Mepron)适用于13岁及以上成人和青少年中无法耐受甲氧苄啶...[ 详情 ]
阿托伐醌(Mepron)适用于13岁及以上成人和青少年中无法耐受甲氧苄啶...[ 详情 ] 非诺贝特片(Lipidil)应在确诊为高脂血症后使用,不可作为高脂血症的预防...[ 详情 ]
非诺贝特片(Lipidil)应在确诊为高脂血症后使用,不可作为高脂血症的预防...[ 详情 ]