2023CSCO指南胃癌免疫治疗:替雷利珠单抗升为Ⅰ级推荐

2013年4月21日-22日,2023 CSCO指南会隆重召开。大会设有多个专场,对指南的更新部分进行讲解。在胃癌专场,北京大学肿瘤医院张小田教授对转移胃癌免疫治疗部分进行了全面解读,主要分为三个更新点,下面一起来了解一下吧!
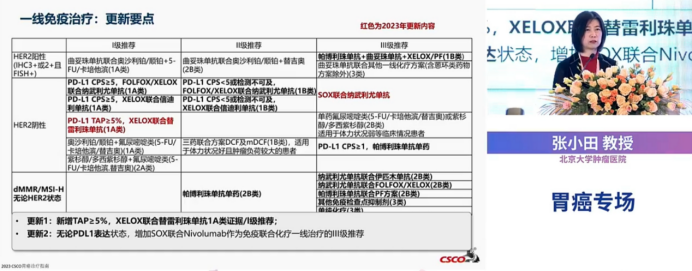
(一)更新一
一线治疗推荐增加XELOX联合替雷利珠单抗,ⅠA类证据和Ⅰ级推荐

RATIONALE 305是一项随机、双盲、安慰剂对照的Ⅲ期试验,用来比较替雷利珠单抗联合铂类和氟嘧啶化疗与安慰剂联合铂类和氟嘧啶化疗作为一线治疗局部晚期、不可切除或转移性胃/胃食管交界处腺癌患者的疗效和安全性。主要终点是PD-L1+和ITT分析人群的总生存期(OS)。
研究结果表明:替雷利珠单抗联合化疗组的中位随访时间为 11.8 个月,安慰剂组为 11.7 个月。与安慰剂组相比,替雷利珠单抗联合化疗组的总生存期( OS )有显著改善(中位总生存期17.2个月 VS 12.6 个月)。与安慰剂组相比,替雷利珠单抗联合化疗组还具有更长的 无进展生存期(PFS)(中位无进展生存期 7.2 个月VS 5.9 个月)、更高的客观缓解率(ORR)(50.4% VS 43.0%)和更持久的反应(中位缓解持续时间 9.0个月 VS 7.1 个月)。
(二)更新二
增加SOX联合Nivolumab作为免疫联合化疗一线治疗的Ⅲ级推荐

ATTRACTION-4 是一项随机、多中心、双盲、安慰剂对照的Ⅲ期临床研究,旨在评估纳武利尤单抗联合化疗与化疗作为 HER2 阴性、晚期或复发性 G/GEJ 癌症患者一线治疗的疗效和安全性。共纳入724名患者,并随机分配(1:1)接受纳武利尤单抗联合化疗或安慰剂联合化疗。每 3 周在静脉给予纳武利尤单抗(360mg)或安慰剂,直至疾病进展或出现不可接受的毒性。试验的主要终点是RECIST委员会评估的无进展生存期(PFS) 和总生存期(OS)。

研究结果表明:中位无进展生存期和中位随访期为 11.6 个月时,纳武利尤单抗联合化疗组与安慰剂组相比无进展生存期(PFS) 有明显改善( 10.5个月VS 8.3 个月),达到了该试验的主要终点。在总生存期(OS)和中位随访期为 26.6 个月时,两组在统计学上的没有明显差异(中位总生存期17.5个月 VS 17.2 个月),但纳武利尤单抗联合化疗组中的无进展生存期比安慰剂组持续时间更长,并且纳武利尤单抗联合化疗组中的客观缓解率(ORR)比安慰剂组高(57.5% VS 47.8%)。
(三)更新三
Claudin18.2 CAR-T证据来源补充
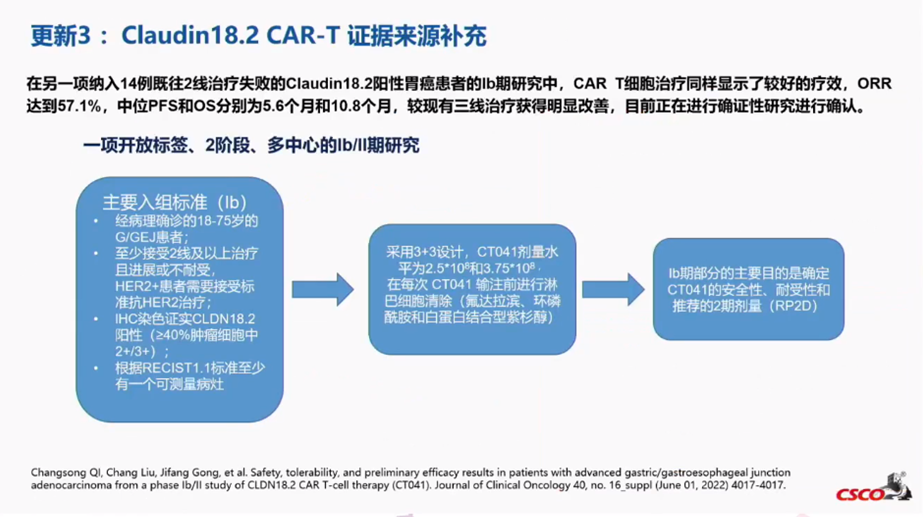
在另一项纳入14例既往2线治疗失败的Claudin18.2阳性胃癌患者的Ⅰb期研究中,CAR T细胞治疗同样显示了较好的疗效,客观缓解率(ORR)达到57.1%,中位无进展生存期(PFS)和总生存期(OS)分别为5.6个月和10.8个月,较现有三线治疗获得明显改善,目前正在进行确证性研究进行确认。
研究结果表明:中位随访时间为8.8(3.0-13.6)个月。在第一次CT041输注后的首次肿瘤评估中,14名患者中有57.1%(8名)实现了部分缓解(PR)。客观缓解率(ORR)达 57.1%,疾病控制率(DCR)达78.6%,中位无进展生存期(mPFS) 5.6个月,中位生存期(mOS)10.8个月。
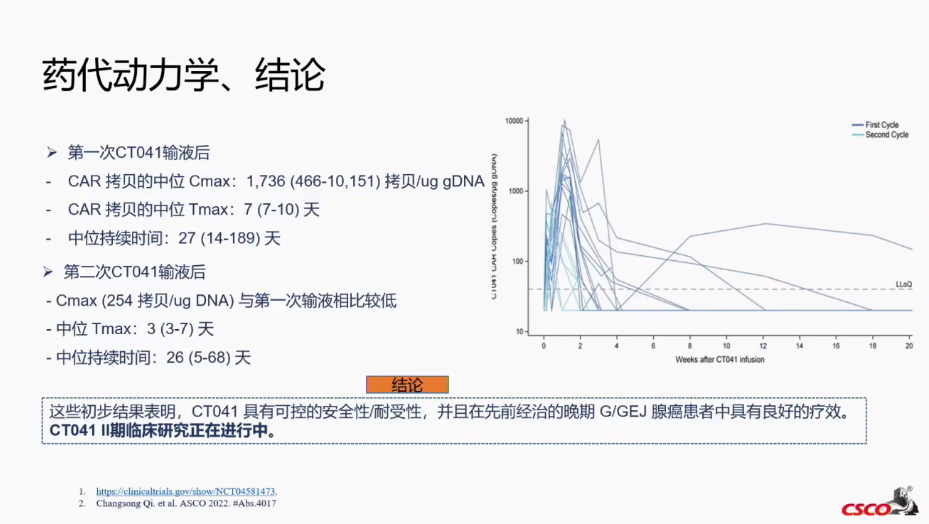
这些研究的初步结果表明,CT041具有可控的安全性/耐受性,并且在先前经治的晚期G/GEJ腺癌患者中具有良好的疗效。cT041 Ⅱ期临床研究正在进行中。

免疫联合化疗(±靶向治疗)在晚期胃癌一线治疗中逐渐成为标准,之后还有更多研究值得我们关注,大家一起来期待吧!
参考文献:
(1)Kang YK, Chen LT, Ryu MH, Oh DY, Oh SC, Chung HC, Lee KW, Omori T, Shitara K, Sakuramoto S, Chung IJ, Yamaguchi K, Kato K, Sym SJ, Kadowaki S, Tsuji K, Chen JS, Bai LY, Oh SY, Choda Y, Yasui H, Takeuchi K, Hirashima Y, Hagihara S, Boku N. Nivolumab plus chemotherapy versus placebo plus chemotherapy in patients with HER2-negative, untreated, unresectable advanced or recurrent gastric or gastro-oesophageal junction cancer (ATTRACTION-4): a randomised, multicentre, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2022 Feb;23(2):234-247. doi: 10.1016/S1470-2045(21)00692-6. Epub 2022 Jan 11. PMID: 35030335.
(2)Qi C, Gong J, Li J, Liu D, Qin Y, Ge S, Zhang M, Peng Z, Zhou J, Cao Y, Zhang X, Lu Z, Lu M, Yuan J, Wang Z, Wang Y, Peng X, Gao H, Liu Z, Wang H, Yuan D, Xiao J, Ma H, Wang W, Li Z, Shen L. Claudin18.2-specific CAR T cells in gastrointestinal cancers: phase 1 trial interim results. Nat Med. 2022 Jun;28(6):1189-1198. doi: 10.1038/s41591-022-01800-8. Epub 2022 May 9. PMID: 35534566; PMCID: PMC9205778.
 本内容由 国家中医药管理局名词术语成果转化与规范推广项目 审核认证
本内容由 国家中医药管理局名词术语成果转化与规范推广项目 审核认证
- 【多囊肾病伴高血压】经肾动脉去交感神经术(RDN)[适 应 症]高血压[试验分期]Ⅰ期
- 【抑郁症】盐酸(R)氯胺酮[适 应 症]抑郁症[试验分期]Ⅰ期,Ⅱ期
- 【CD38+血液肿瘤】SCTC21C[适 应 症]淋巴瘤,淋巴瘤/白血病[试验分期]Ⅰ期
- 【KRASG12C突变实体瘤】GH21胶囊联合D-1553片[适 应 症]肺癌,结直肠癌,实体瘤[试验分期]Ⅰ期,Ⅱ期
- 【EGFR 20ins肺癌】JMT101联合奥希替尼[适 应 症]肺癌[试验分期]Ⅲ期
- 【NTRK实体瘤】Repotrectinib 瑞普替尼[适 应 症]肝癌,乳腺癌,宫颈癌,卵巢癌,胃癌,前列腺癌,食道癌,实体瘤,食管癌,胆道癌,头颈部鳞状细胞癌,子宫内膜癌,胃或GEJ腺癌,尿路上皮癌,胸腺癌,食管鳞癌[试验分期]Ⅱ期
添加医学顾问
做您身边的贴心健康咨询管家

了解医药信息 关注临床动态
- 1阿那白滞素全网公布的2024年的最新价格已帮助人数12人2024-07-26 18:01
- 2佐妥昔单抗不同版本一盒的最新价格公布已帮助人数15人2024-07-26 17:40
- 3阿那白滞素导致的不良反应怎么治疗已帮助人数11人2024-07-26 17:27
- 4佐妥昔单抗全网公布的2024年的最新价格已帮助人数12人2024-07-26 17:25
- 5佐妥昔单抗正品有合适的购买方式吗?已帮助人数23人2024-07-26 17:06
- 6阿那白滞素仿制药的正确购买途径已帮助人数10人2024-07-26 16:53
- 7佐妥昔单抗全新购买方式一览已帮助人数14人2024-07-26 16:31
- 8阿那白滞素在中国上市了吗?好购买吗已帮助人数11人2024-07-26 16:20
- 9佐妥昔单抗导致的不良反应怎么治疗?已帮助人数12人2024-07-26 15:52
- 10佐妥昔单抗在中国上市了吗?好购买吗?已帮助人数15人2024-07-26 15:27
- 11佐妥昔单抗仿制药的正确购买途径已帮助人数12人2024-07-26 14:44
- 12佐妥昔单抗仿制版也能有效治病吗?已帮助人数18人2024-07-26 13:38
 匹米替比(Pimitespib)匹米替比适用于已经接受过伊马替尼、舒尼替...[ 详情 ]
匹米替比(Pimitespib)匹米替比适用于已经接受过伊马替尼、舒尼替...[ 详情 ] Tarlatamab-dlle(塔拉妥单抗、IMDELLTRA)适用于治疗在铂类化疗期间或之后疾病进展的...[ 详情 ]
Tarlatamab-dlle(塔拉妥单抗、IMDELLTRA)适用于治疗在铂类化疗期间或之后疾病进展的...[ 详情 ] 奥氮平片(Zyprexa)1、奥氮平用于治疗精神分裂症。 2、初...[ 详情 ]
奥氮平片(Zyprexa)1、奥氮平用于治疗精神分裂症。 2、初...[ 详情 ] 克立硼罗(舒坦明、Crisaborole)克立硼罗(舒坦明、Crisaborole...[ 详情 ]
克立硼罗(舒坦明、Crisaborole)克立硼罗(舒坦明、Crisaborole...[ 详情 ]




































