维奈托克治疗慢性淋巴细胞白血病的结果和管理:美国真实世界研究

维奈托克(venetoclax,Venclyxto)是一种口服第二代B细胞淋巴瘤-2蛋白(BCL2)抑制剂,适用于染色体17p缺失(del(17p))、氟达拉滨耐药、伊布替尼或idelalisib治疗期间或治疗后进展的复发/难治性(R/R)慢性淋巴细胞白血病(CLL)。
CLL患者中维奈托克的疗效、剂量递增和不良事件数据几乎全部来自临床试验。本研究的目的是更好地了解真实世界临床实践中使用维奈托克治疗的CLL患者的疾病特征和不良事件。研究人员探讨了维奈托克治疗早期进展的预后因素,重点关注维奈托克停药后的结果,并分析了停药后的治疗选择。
患者特征
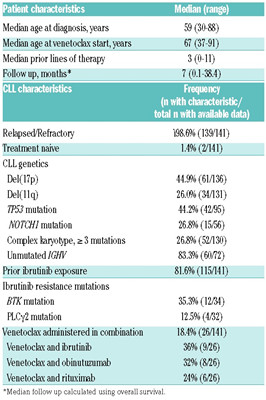
确定了141名接受维奈托克治疗的CLL患者。男性和白人占大多数,比例分别为66%和87%。诊断时患者的中位年龄为59岁(范围30-88),开始维奈托克治疗时的中位年龄为67岁(范围37-91)。患者人群几乎全部由R/R CLL患者组成,只有2名(141%的141%)患者既往未接受过治疗。患者接受了中位数3种(范围0-11)治疗。18.4%(141名患者中的26名)的患者使用维奈托克联合治疗。维奈托克常与伊布替尼(36%),obinutuzumab(32%)和利妥昔单抗(24%)联合使用。在维奈托克治疗前,几乎89%的患者接受了B细胞受体信号转导抑制剂治疗;82%(n=115/141)接受了伊布替尼治疗。患者特征总结在上表中。
该队列中的大多数患者具有至少一种传统上风险较低的特征:45%(n=61/136)患者染色体del(17p),26%(n=34/131)染色体11q缺失(del(11q)),44%(n=42/95)p53突变,26.8%(n=52/130)复杂核型异常(>3种染色体异常),26.8%(n=15/56)NOTCH1突变。31名患者(22%)同时存在del(17p)和TP53突变,16名患者(11%)存在del(17p)、TP53突变和复杂核型异常。
维奈托克给药和不良事件(AE)
对所有患者均进行了5周的维奈托克剂量递增。在剂量递增期间,85%(n=120/141)的患者达到最大日剂量400mg,75%(n=103/137)维持400mg作为长期稳定剂量。30%的患者出现剂量中断,21%的患者需要减少剂量。
血液学事件是最常见的AE,近半数患者(47.4%,n=65/137)发生中性粒细胞减少症(定义为ANC<1000细胞/微升),三分之一的患者(36.0%,n=49/136)报告血小板减少症。其他AE包括肿瘤溶解综合征(TLS)(13.4%,n=18/134),中性粒细胞减少性发热(11.6%,n=16/138)和≥2级腹泻(7.3%,n=10/138)。维奈托克治疗期间11名患者(7.8%)报告了机会性感染,其中最常见的是肺孢子虫肺炎(PJP)(n=6),侵袭性真菌(n=2)和弓形虫病(n=2)。先前接受过激酶抑制剂治疗的患者发生了9例机会性感染,之前接受过伊布替尼治疗的患者发生了8例机会性感染,而接受过上述两种激酶抑制剂治疗的患者发生了6例机会性感染。从维奈托克开始到发生机会性感染的中位时间是5个月(0.2-16个月)。
肿瘤溶解综合征(TLS):预防和住院
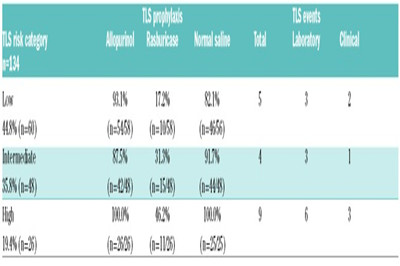
在134名有TLS数据的患者中,44.8%为低风险(n=60),35.8%为中度风险(n=48),19.4%为高风险(n=26)。有89名(64.3%)在维奈托克治疗前通过CT扫描进行了淋巴结评估。为了尽量减少TLS的发生,几乎所有患者应用别嘌呤醇(低风险患者93.1%,中度风险87.5%,高风险100.0%),静脉注射生理盐水的患者比例类似(低风险82.1%,中度风险91.7%,高风险100.0%)。使用Rasburicase预防TLS的情况不同:低风险17.2%,中度风险31.3%,高风险46.2%。
在剂量递增期间,无论风险类别如何,大多数患者都进行过一次或多次住院治疗。27名患者没有住院,低风险患者20/58名患者(34.5%),中度风险7/48名患者(14.6%)。在剂量递增阶段,所有高风险患者至少住院一次以监测和预防TLS。剂量递增期间低风险,中度风险和高风险患者住院的平均天数分别为1.5,1.7和3.1天。
总体而言,(实验室和临床)TLS事件的发生率为13.4%(n=18/134),其中5例事件(3.7%)发生在低风险患者中,4例(3.0%)发生在中度风险患者中,9例(6.7%)发生在高风险患者中。在这些事件中,6例为临床TLS事件(2名低风险患者,1名中度风险患者和3名高风险患者;其中4名维奈托克给药剂量400mg),其余为实验室事件(n=12)。没有TLS患者需要血液透析。
治疗结果
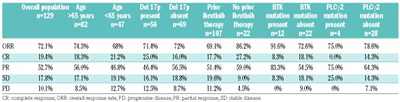
整个队列的客观反应率(ORR)为72.1%,19.4%的患者达到完全反应(CR)。至最佳反应的中位时间为2.1个月。在以下高风险组中维奈托克的ORR相似:年龄≥65(ORR=74.3%),del(17p)(71.4%),接受过伊布替尼治疗(69.1%),BTK突变(91.6%)和PLCγ2突变(75.0%)患者。

在7个月的中位随访期间,整个队列的中位PFS和OS尚未达到。12个月时,整个队列的预计无进展生存率和总生存率分别为68%和88%。TP53不完整【del(17p)和/或TP53突变】患者的PFS显著短于其他患者,而OS没有显著差异。
在单变量分析中,TP53不完整是PFS较差的预测因子(HR 2.7,95%CI 1.08-6.7,P=0.034),但不是OS的预测因子(HR 1.78,95%CI.55-5.74,P=.332)。复杂核型异常(HR 1.36,95%CI 0.66-2.84,P=0.4),接受过伊布替尼治疗(1.74,95%CI 0.61-5.0,P=0.3)和IGHV未突变(HR 0.29,95%CI 0.04-2.3,P=0.25)与PFS较差无显著相关性。包括TP53中断,复杂核型异常和伊布替尼治疗的多变量分析中,TP53中断仍然是PFS较差的重要预测指标(HR 2.8,CI 1.22-6.4,P=0.03)。del(11q)的存在不影响OS,且对PFS有保护作用(HR 0.31,95%CI 0.11-0.90,P=0.03)。
维奈托克停药和停药之后的治疗选择
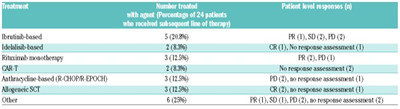
41名患者(29%)停用维奈托克。停药最常见的原因是疾病进展(53.8%,n=21),其次是不良事件(20.5%,n=9),其中三分之二是血液学不良事件。停药的其他原因包括:与进展疾病无关死亡(10.25%,n=4),第二癌(5.1%,n=2),医生/患者偏好(2.5%,n=1),Richter's综合征转化(2.5%,n=1),计划的替代疗法包括靶向CD19的嵌合抗原受体T细胞(CAR-T,2.5%,n=1)和移植(2.5%,n=1)。上表总结了维奈托克治疗后患者的治疗选择和结果。
值得注意的是,患者中有17名(50%)停用维奈托克并且仍然存活,并不需要进行后续治疗。在停用维奈托克后尚未接受治疗的患者停药的原因包括:不良事件(n=6),CLL进展(n=4),继发于不良事件或进展的死亡(n=4),继发性恶性肿瘤(n=2),以及医生或患者偏好(n=1)。维奈托克停药后最常见的治疗选择是含伊布替尼疗法;24名患者中有5名(21%)接受伊布替尼治疗。用伊布替尼治疗的5名患者中有3名先前接受过伊布替尼治疗。在这5名患者中,1名患者部分反应,2名患者病情稳定,2名患者疾病进展。选择的其他疗法包括:利妥昔单抗单药治疗(12.5%,n=3),含蒽环类药物疗法(12.5%,n=3),同种异体干细胞移植(12.5%,n=3),含idelalisib疗法(8.3%,n=2)和CAR-T疗法(8.3%,n=2)。
本内容为医伴旅版权所有,转载请注明出处。
医伴旅:寻找优质医疗资源,伴您走上康复之旅