K药何时上市的呢?

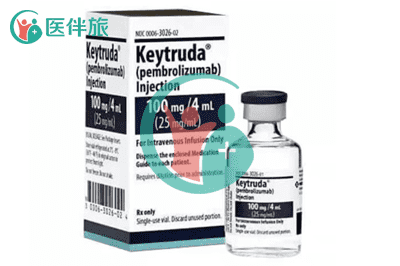
K药(帕博利珠单抗,可瑞达)在中国获批的第一个适应症是不可切除或转移性黑色素瘤,是中国黑色素瘤治疗领域中第一个获批的抗PD-1单抗;与此同时,K药(帕博利珠单抗,可瑞达)也是跨国药企目前唯一在中国开展黑色素瘤临床试验研究的抗PD-1单抗。今天咱们就来详细了解一下K药(帕博利珠单抗,可瑞达)何时上市的呢?
2018年7月,K药(帕博利珠单抗,可瑞达)在中国获批上市,批准的适应症是治疗晚期黑色素瘤。2019年4月,中国扩大了K药(帕博利珠单抗,可瑞达)的治疗适应症,K药(帕博利珠单抗,可瑞达)联合化疗药被用于治疗非小细胞肺癌中的非鳞癌。K药(帕博利珠单抗,可瑞达)终于进入肺癌的治疗。而在国外,K药(帕博利珠单抗,可瑞达)被批准治疗的癌症多达20多种。
K药(帕博利珠单抗,可瑞达)是最先获FDA批准的PD-1单抗药物,于2014年9月获FDA批准上市,随后在2015年和2016年分别在欧洲和日本获批。
在美国,治疗黑色素瘤方面:
(1)K药(帕博利珠单抗,可瑞达)适用于不可切除性或转移性黑色素瘤患者的治疗,推荐给药方案为每3周一次静脉输注200mg,直至病情进展或不可接受的毒性;
(2)K药(帕博利珠单抗,可瑞达)适用于淋巴结受累黑色素瘤患者完全手术切除后的辅助治疗,推荐给药方案为每3周一次静脉输注200mg,直至病情复发或不可接受的毒性,在无疾病复发患者中最多治疗12个月。采用辅助治疗进行早期干预已被证明是降低高危3期黑色素瘤术后复发风险的重要因素。
2019年6月2日,在美国芝加哥召开的ASCO(美国临床肿瘤协会)大会上,PD-1抗体药K药(帕博利珠单抗,可瑞达)的五年生存数据正式公布了。晚期肺癌患者生存率提高了3倍。
这个数据,来自临床试验KEYNOTE-001,患者是晚期非小细胞肺癌,使用的是K药(帕博利珠单抗,可瑞达)单药治疗。这是K药(帕博利珠单抗,可瑞达)最早开始的临床试验,所以对患者的随访时间最长,得到的这个数据,也是目前史上最长的患者使用K药(帕博利珠单抗,可瑞达)治疗之后的生存数据。
使用K药(帕博利珠单抗,可瑞达),把晚期非小细胞肺癌患者的长期生存率整体提高3倍!
以上就是K药(帕博利珠单抗,可瑞达)上市时间的内容,希望可以帮助到您!