英飞凡国内上市没?

阅读量:136
2020-06-12 12:25
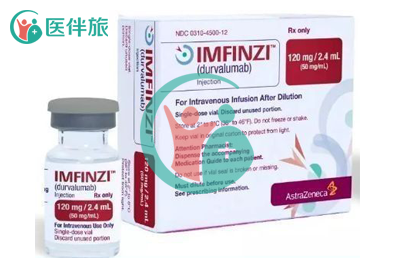
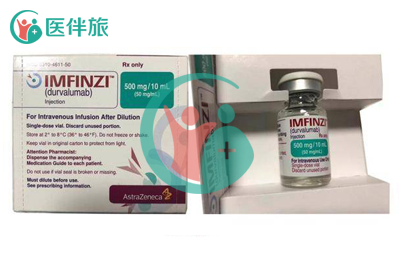
英飞凡国内上市没?2019年12月9日,度伐鲁单抗注射液(英飞凡)获中国国家药品监督管理局批准上市,用于治疗同步放化疗后未进展的不可切除III期非小细胞肺癌。这也是第1个在中国上市的PD-L1单抗。
下面来看看英飞凡的上市历程吧。
英飞凡由阿斯利康公司生产,早在2017年英飞凡首次获得FDA批准用于局部晚期或转移性尿路上皮癌。
2018年2月英飞凡获得美国食品和药物管理局(FDA)的批准,作为非小细胞肺癌第三期患者的一种新的标准治疗方案。这种通过静脉注射的疗法,通过阻断一种叫做PD-L1(程序性细胞死亡配体1)的蛋白质,帮助增加T细胞的活化。

2019年7月12日,美国FDA授予英飞凡孤儿药资格认定,用于小细胞肺癌(SCLC)的治疗。
2020年3月30日,美国FDA正式批准PD-L1免疫治疗药度伐利尤单抗(英飞凡)成为小细胞肺癌的一线治疗用药!英飞凡新批的适应症是:联合化疗用于未经系统治疗的广泛期小细胞肺癌患者的治疗。
在PACIFIC研究中,采用英飞凡巩固治疗含铂同步放化疗后疾病尚未进展的局部晚期或不可切除的III期非小细胞肺癌(NSCLC)患者。和安慰剂相比,英飞凡中位PFS(无进展生存空间)是16.8 : 5.6个月,延长11.2个月!英飞凡治疗既往含铂治疗失败晚期尿路上皮癌患者,整体效果对比是17.8%,PD-L1高表达(≥25%)患者的效果对比达到27.6%。总体中位生存时间是18.2个月,PD-L1高表达的患者中位OS(总生存期)是20个月。
下一篇: Stivarga是什么?
相关药讯
最新药讯
肺癌用药

正品保障
正品保障 放心选购

厂家直采
厂家授权 正品渠道

专业药师
一对一用药指导

品类齐全
海外药房 药品齐全
微信客服
企业微信
联系我们 :24小时客服在线
400-001-2811

邮箱 : service@1blv.com
邮编 : 100096
地址 : 北京市昌平区珠江摩尔国际大厦3号楼2单元701室
本网站不销售任何药品,只做药品信息资讯展示
证书编号:(京)-非经营性-2020-0182 互联网药品信息服务资格证书