Bylvay精准“打击”进行性家族性肝内胆汁淤积症!疗效显著!
公开资料显示,进行性家族性肝内胆汁淤积症1型和 2型发病率为1/100 000~ 1/50 000,发病与性别无关,而Bylvay 作为美国第一个获批用于治疗所有类型进行性家族性肝内胆汁淤积症的药物,疗效如何?随小编一起来看看吧!
进行性家族性肝内胆汁淤积症
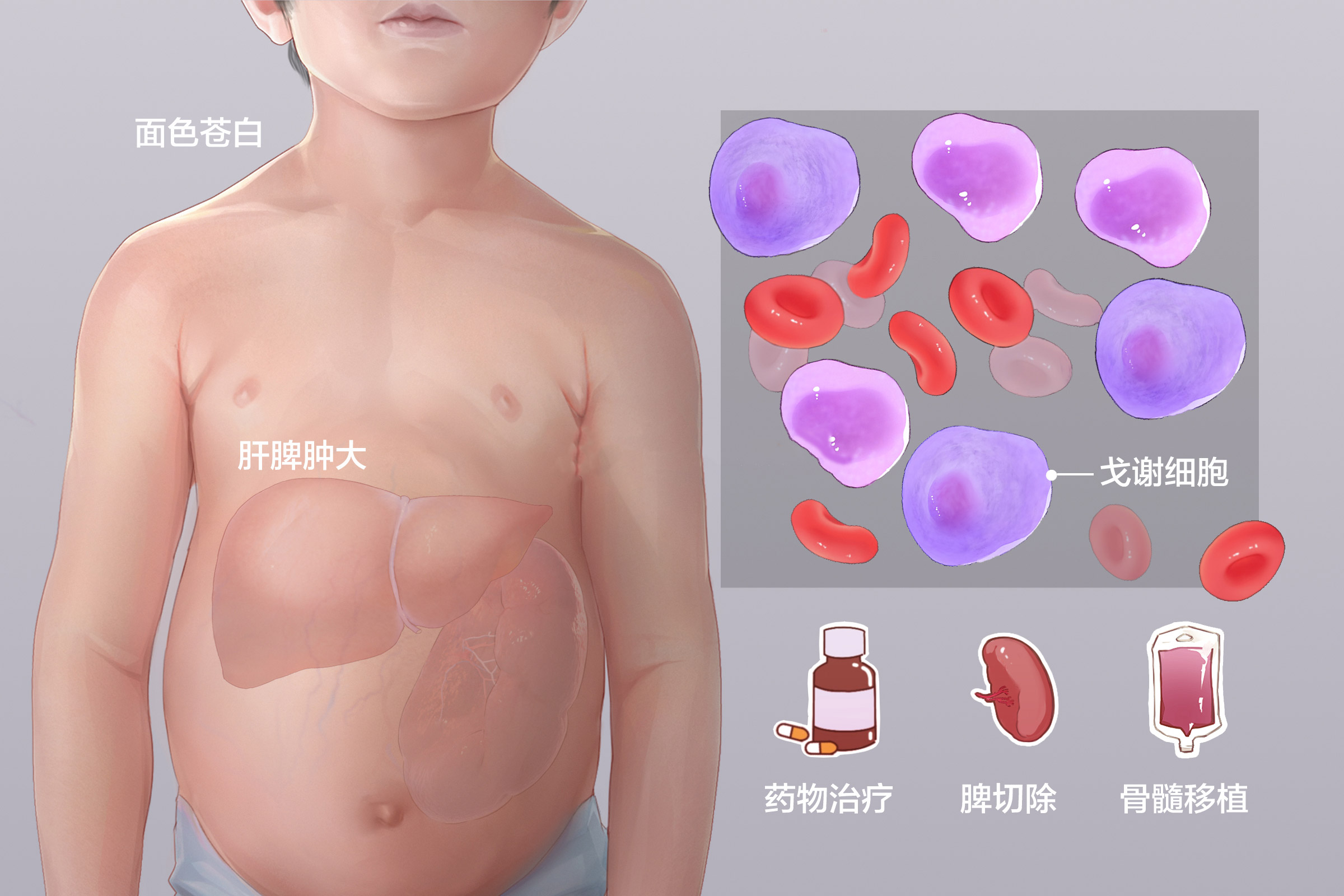
进行性家族性肝内胆汁淤积症(PFIC)是一种常染色体隐性遗传病。肝脏合成、分泌胆汁,胆汁在胆囊浓缩、储存。当人体摄入脂肪类食物,胆囊会分泌胆汁,帮助脂肪的消化。本病患者是由于基因突变,导致肝内胆汁分泌障碍,发生肝内胆汁淤积,最终发展为肝衰竭。患者典型症状有黄疸和皮肤瘙痒,还有发育落后、身材矮小等问题。
根据致病基因不同,进行性家族性肝内胆汁淤积症主要分为3型,分别为PFIC-1 型:由位于常染色体18q21-22的ATP8B1基因突变所致,其功能异常可间接干扰胆管胆汁酸分泌。患者常有水样腹泻、胰腺炎、听力减退。PFIC-2型:由位于常染色体2q24的ABCB11基因突变所致,会导致肝细胞内胆盐积聚,造成肝脏损伤,初始表现严重,进展最快,1年内可迅速发展呈肝衰竭。PFIC-3 型:由 ABCB4 基因突变引起,可导致胆结石形成,阻塞胆道胆汁排泄。这一型一般呈慢性进展,常在儿童晚期和青少年发生肝硬化。
Bylvay(odevixibat)
Bylvay 是美国第一个获批用于治疗所有类型进行性家族性肝内胆汁淤积症 (PFIC) 的 3 个月及以上患者瘙痒症的药物。欧盟委员会 (EC) 和英国药品和保健品监管机构 (MHRA) 还授予了 Bylvay 的上市许可,用于治疗 6 个月或以上患者的 PFIC。
Bylvay 是一种有效的、每日一次的非全身性回肠胆汁酸转运抑制剂,全身暴露量最小,并在小肠局部起作用。对于能够吞咽胶囊的患者,Bylvay 可以作为胶囊服用,也可以打开并洒在食物上,这是儿科患者人群依从性的关键因素。Bylvay 最常见的不良反应是腹泻、肝功能检查异常、呕吐、腹痛和脂溶性维生素缺乏。
Bylvay疗效
2022年6月,《Lancet Gastroenterol Hepatol》发布了一项 24周、随机、双盲、已完成的Ⅲ期试验,其目的为探究odevixibat的疗效,已知进行性家族性肝内胆汁淤积症的主要症状为瘙痒和血清胆汁酸升高,因此两个主要终点即为24周内瘙痒阳性和血清胆汁酸反应阳性的患者比例。
将试验纳入的患者随机分配(1:1:1),给予每天一次安慰剂,40μg/kg和120μg/kg的odevixibat。与安慰剂相比,24周治疗期间,瘙痒评估呈阳性的患者比例为:总体odevixibat组与安慰剂组的绝对比例差异为为55%;odevixibat的40μg/kg/d组为58%;120μg/kg/d组为52%,详细数据如图A:
图A:瘙痒评估呈阳性的患者比例
血清胆汁酸阳性的患者比例为:在接受odevixibat治疗的所有42例患者中,14例(33%)呈血清胆汁酸阳性,其中40μg/kg/d组的23例中有10例(43%);120μg/kg/d组的有19例中有4例(21%),而接受安慰剂的患者(20例中有0例)达到该反应阈值,总体odevixibat组与安慰剂组的绝对比例差异为33.3%,详细数据如图B:
图B:血清胆汁酸阳性的患者比例
综上所述,与安慰剂相比,全odevixibat组患者水平瘙痒和血清胆汁酸的阳性评估的患者比例均高于安慰剂,疗效十分显著!
进行性家族性肝内胆汁淤积症药物全球研发
目前针对进行性家族性肝内胆汁淤积症的药物,除了已上市的odevixibat外,还有13种药物,目前处于非在研阶段的药物有1种,药物发现阶段的有3种药物,临床前阶段的有4种,临床2期的有1种,临床3期的目前有2种,申请上市的有1种,相信在不久的将来就会与我们见面,此外还有1种已出现在大家面前的药物,今天就为大家简单介绍一下:
氯马昔巴特(Maralixibat Chloride)
氯马昔巴特(maralixibat)由美国Mirum制药公司研发,于2021年9月29日经FDA优先审查方式批准上市,商品名为Livmarli,用于治疗1岁及以上的Alagille综合征(ALGS)患者的胆汁淤积性瘙痒.本品为口服液体制剂,是FDA批准的第一个也是唯一一个治疗ALGS这种罕见肝病的药物。
氯马昔巴特口服溶液是一种口服、每日一次的回肠胆汁酸转运蛋白(IBAT)抑制剂,它可以阻断胆汁酸肠肝循环,降低肝内和血清中的胆汁酸水平,减少由此介导的肝脏损伤,缓解瘙痒。
参考文献
[1]Thompson RJ, Arnell H, Artan R, Baumann U, Calvo PL, Czubkowski P, Dalgic B, D'Antiga L, Durmaz Ö, Fischler B, Gonzalès E, Grammatikopoulos T, Gupte G, Hardikar W, Houwen RHJ, Kamath BM, Karpen SJ, Kjems L, Lacaille F, Lachaux A, Lainka E, Mack CL, Mattsson JP, McKiernan P, Özen H, Rajwal SR, Roquelaure B, Shagrani M, Shteyer E, Soufi N, Sturm E, Tessier ME, Verkade HJ, Horn P. Odevixibat treatment in progressive familial intrahepatic cholestasis: a randomised, placebo-controlled, phase 3 trial. Lancet Gastroenterol Hepatol. 2022 Sep;7(9):830-842. doi: 10.1016/S2468-1253(22)00093-0. Epub 2022 Jul 1. PMID: 35780807.
[2]Srivastava A Progressive familial intrahepatic cholestasis.J Clin Exp Hepatol. 2014; 4: 25-36
[3]Bull LN Thompson RJ Progressive familial intrahepatic cholestasis.Clin Liver Dis. 2018; 22: 657-669
已帮助人数261人
2023-07-11 16:38