



艾萨妥昔单抗(Isatuximab)
艾萨妥昔单抗(Isatuximab)
中文名称:艾萨妥昔单抗
英文名:Isatuximab
商品名:SARCLIS
适应症
SARCLISA是一种CD38定向的细胞溶解抗体,适用于:
(1)与泊马利度胺和地塞米松联合治疗多发性骨髓瘤的成年患者,这些患者至少接受过2次治疗,包括来那度胺和蛋白酶体抑制剂。
(2)联合卡非佐米和地塞米松治疗复发或难治性多发性骨髓瘤的成年患者,这些患者之前接受过1到3次治疗。
用法用量
用法:静脉注射。在输注SARCLISA前15 - 60分钟进行以下药物预处理,以降低输注相关反应的风险和严重程度。
①SARCLISA和泊马度胺联合使用时: 40mg地塞米松口服或静脉注射(或对于≥75岁的患者,20mg口服或静脉注射)。
②SARCLISA和卡菲佐米联合用药时:20mg地塞米松(SARCLISA和/或卡菲佐米输注时静脉注射,在第2周期及以后的第22天口服,在所有周期的第23天口服)
③口服醋氨酚650 mg至1000 mg(或同等剂量)。
④H2拮抗剂
⑤苯海拉明25 mg至50 mg口服或静脉注射(或同等剂量)。
用量: SARCLISA的推荐剂量为每周静脉输注10 mg/kg,持续4周,然后每2周一次,直到疾病进展或出现不可接受的毒性。
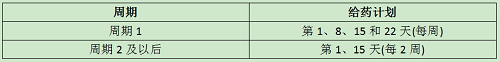
每个治疗周期为28天。重复治疗,直到疾病进展或不可接受的毒性。
规格
SARCLISA是一种透明至微乳白色、无色至微黄色的溶液,基本上不含可见颗粒,包括3种剂型:
(1)注射:100mg / 5ml (20mg /mL),单剂量瓶
(2)注射:500mg / 25ml (20mg /mL),单剂量瓶
不良反应
(1)联合泊马利度胺和地塞米松使用:最常见的不良反应(≥20%)为上呼吸道感染、输液相关反应、肺炎和腹泻。输液相关反应严重的体征和症状包括心跳骤停、高血压、低血压、支气管痉挛、呼吸困难、血管水肿和肿胀。最常见的血液学实验室异常(≥80%)为血红蛋白减少、中性粒细胞减少、淋巴细胞减少、血小板减少。在接受Sarclisa方案治疗的患者中,第二原发恶性肿瘤的发病率增加。
(2)联合卡非佐米和地塞米松使用:最常见的不良反应(≥20%)为上呼吸道感染、输液相关反应、疲劳、高血压、腹泻、肺炎、呼吸困难、失眠、支气管炎、咳嗽和背痛。输液相关反应严重的体征和症状包括心跳骤停、高血压、低血压、支气管痉挛、呼吸困难、血管水肿和肿胀。最常见的血液学实验室异常(≥80%)为血红蛋白、淋巴细胞和血小板减少。在接受Sarclisa方案治疗的患者中,第二原发恶性肿瘤的发病率增加。在所有接触SARCLISA的患者中,继发性原发性恶性肿瘤的总发病率为3.6%。
禁忌
对isatuximab irfc或其任何赋形剂严重过敏的患者禁用SARCLISA。
注意事项
(1)在儿科患者中的安全性和有效性尚未确定。
(2)孕妇使用SARCLISA可能会导致胎儿伤害,建议有生育计划的女性患者在治疗期间和最后一次接受SARCLISA治疗后至少5个月内采取有效的避孕措施。
(3)由于isatuximab-irfc和泊马度胺、地塞米松联合使用可能会对母乳喂养的婴儿造成严重的不良反应,建议哺乳期妇女在接受SARCLISA治疗期间不进行母乳喂养。
贮藏
将药箱在36°F至46°F(2°C至8°C)下冷藏,注意避光。不要冷冻。不要摇晃。
作用机制
Isatuximab-irfc是一种CD38靶向的细胞溶解抗体,是嵌合免疫球蛋白G1 (IgG1)单克隆抗体(mAb)。isatuximb -irfc是由哺乳动物细胞系(中国仓鼠卵巢,CHO)使用饲料批量生产工艺生产的。Isatuximab-irfc由两个相同的免疫球蛋白kappa轻链和两个相同的免疫球蛋白gamma重链组成,总体分子量约为148 kDa。
SARCLISA (isatuximab-irfc)注射剂是一种无菌,不含防腐剂,透明到略呈乳白色,无色到略黄色的溶液,在静脉使用的单剂量瓶中基本上不含可见颗粒。每瓶含有100mg / 5ml或500mg / 25ml的isatuximab-irfc,浓度为20mg /mL, pH为6.0。每毫升溶液含有20mg isatuximab-irfc、组氨酸(1.46 mg)、一水组氨酸盐酸盐(2.22 mg)、聚山梨酯80 (0.2 mg)、蔗糖(100 mg)和注射用水。
安全与疗效
(1)ICARIA-MM (NCT02990338)试验评估了SARCLISA联合泊马度胺和地塞米松(Isa-Pd)的有效性和安全性,这是一项多中心、多国界、随机化、开放标签、2组对照的3期临床试验,研究对象为复发和/或难治性多发性骨髓瘤患者。这些患者之前至少接受过两种治疗,包括来那度胺和蛋白酶体抑制剂。符合条件的患者为:ECOG)评分为0-2、血小板≥75,000 cells/mm3、绝对中性粒细胞计数≥1 × 109/L、肌酐清除率≥30 mL/min/1.73 m2 (MDRD公式)、AST≤3 ×ULN、ALT≤3×ULN。
307例患者按1:1的比例随机接受SARCLISA联合泊马度胺和地塞米松(Isa-Pd, 154例)或泊马度胺和地塞米松(Pd, 153例)。两组均以28天为一个周期进行治疗,直到疾病进展或出现不可接受的毒性。SARCLISA在第一个周期的每周以及随后周期每2周以 10 mg/kg的剂量静脉滴注给药。泊马度胺在每个28天周期的第1天到第21天口服,每天4 mg。地塞米松在每个28天周期的第1、8、15和22天口服或静脉注射给药,剂量为40 mg(年龄≥75岁的患者20 mg)。
总体而言,两组患者基线时的人口学和疾病特征相似。患者中位年龄为67岁(范围36-86),20%的患者年龄≥75岁;79%的患者是白人,12%是亚洲人,1%是黑人或非洲裔美国人;10%的患者有COPD或哮喘病史。肾损害(肌酐清除率<60 mL/min/1.73 m2)患者比例为34%。在研究开始时,国际分期系统(ISS)分期为I期的患者占37%,II期患者占36%,III期患者占25%。总体而言,在研究开始时,20%的患者有高危染色体异常;Del (17p)、t(4;14)和t(14;16)分别在12%、8%和2%的患者中存在。
既往治疗次数的中位数为3次(范围2-11)。所有患者之前都接受过蛋白酶体抑制剂、来那度胺,56%的患者之前接受了干细胞移植;大多数患者(93%)对来那度胺耐药,76%对蛋白酶体抑制剂耐药,73%对免疫调节剂和蛋白酶体抑制剂均耐药。
Isa-Pd组的中位治疗持续时间为41周,而Pd组为24周。
SARCLISA的疗效评估是基于无进展生存期(PFS)。PFS结果由一个独立的反应委员会根据中央实验室的m蛋白数据和采用国际骨髓瘤工作组(IMWG)标准的中央影像学评价进行评估。在接受Isa-Pd治疗的患者中,PFS的改善表明疾病进展或死亡风险降低了40%。
Isa-Pd组第一次缓解的中位时间为35天,而Pd组为58天。IsaPd组的中位缓解持续时间为13.3个月(95% CI: 10.6-NR),而Pd组为11.1个月(95% CI: 8.5-NR)。两组患者的中位总生存期均未达到。中位随访时间为11.6个月,Isa-Pd组43例(27.9%)患者死亡,Pd组56例(36.6%)患者死亡。中期分析时OS结果无统计学意义。
疗效对比见下表:
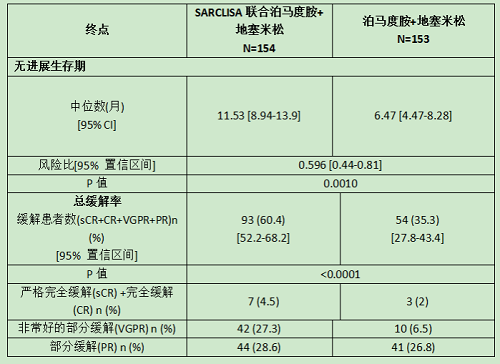
(2)IKEMA (NCT03275285)试验对SARCLISA联合卡非佐米和地塞米松的有效性和安全性进行了评估。这是一项多中心、多国界、随机化、开放标签、2组对照的3期临床试验,研究对象为复发和/或难治性多发性骨髓瘤患者。这些患者前期接受了一到三种治疗方案。符合条件的患者为:ECOG评分为0-2、血小板≥50,000 cells/mm3、绝对中性粒细胞计数≥1× 109/L、肌酐清除率≥15 mL/min/1.73 m2 (MDRD公式)、AST≤3×ULN、ALT≤3×ULN。
302例患者按3:2的比例随机接受SARCLISA联合卡菲佐米和地塞米松(Isa-Kd, 179例)或卡菲佐米和地塞米松(Kd, 123例)。两组均以28天为一个周期进行治疗,直到疾病进展或出现不可接受的毒性。SARCLISA在第一个周期的每周以及随后周期每2周以 10 mg/kg的剂量静脉滴注给药。卡菲佐米的给药:第1、2天静脉滴注20mg /m2 ; 第1个周期的第8、9、15、16天56 mg/m2 ; 随后每个28天周期的第1、2、8、9、15、16天剂量为56 mg/m2。地塞米松在每个28天周期的第1,、2、 8、 9、 15、 16、 22和23天以20 mg的剂量给药(在isatuximab-irfc和/或卡非佐米输注的同一天注射给药,或者是在其他时间口服)。在同时给予SARCLISA和卡非佐米的时候,先给予地塞米松,然后输注SARCLISA,再输注卡非佐米。
总体而言,两组患者基线时的人口学和疾病特征相似。患者中位年龄为64岁(33-90岁),9%≥75岁,71%为白人,17%为亚洲人,3%为黑人或非裔美国人。Isa-Kd组患者出现肾损害(eGFR<60 mL/min/1.73 m2)的患者比例为24%,Kd组为15%。在研究开始时,国际分期系统(ISS)分期为I期的患者占53%,II期的患者占31%,III期的患者占15%。总体而言,24%的患者在研究开始时有高危染色体异常;Del (17p)、t(4;14)、t(14;16)分别在11%、14%和2%的患者中存在。此外,42%的患者出现增益(1q21)。
既往治疗次数的中位数为2(范围1-4),44%的患者曾接受过1次前期治疗。总的来说,90%的患者接受了蛋白酶体抑制剂治疗,78%的患者接受了免疫调节剂治疗(包括43%的患者接受了来那度胺治疗),61%的患者接受了干细胞移植治疗。总体而言,33%的患者对之前的蛋白酶体抑制剂难治,45%的患者对之前的免疫调节剂难治(包括33%的来那度胺难治),21%的患者对蛋白酶体抑制剂和免疫调节剂都难治。
Isa-Kd组的中位治疗持续时间为80周,Kd组为61周。
SARCLISA的疗效评估是基于PFS。PFS结果由独立反应委员会根据中央实验室的m蛋白数据和采用IMWG标准的中央影像学复查评估。与Kd治疗的患者相比,采用Isa-Kd治疗的患者PFS的改善意味着疾病进展或死亡的风险降低了45%。
疗效对比见下表:
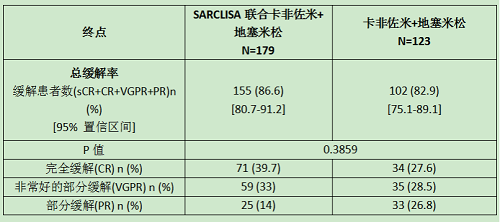
【完整说明书详见】:https://nctr-crs.fda.gov/fdalabel/ui/search













 医伴旅服务热线:
医伴旅服务热线:








