阿柏西普什么时候上市?

阅读量:175
2020-06-24 09:36
阿柏西普是全球首个完全人源化的融合蛋白,一种可与VEGF-A、PlGF结合的可溶性诱饵受体,可抑制内源性VEGF受体与VEGF-A和PlGF的结合和激活。阿柏西普什么时候上市?
2012年,美国FDA批准阿柏西普(Zaltrap)治疗转移性结直肠癌。该适应症是联合传统的FOLFIRI方案(伊立替康、亚叶酸钙、5-氟尿嘧啶)二线治疗已使用含奥沙利铂方案疾病出现进展的病人。

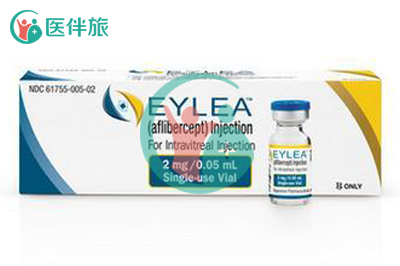
国家食品药品监督管理总局药品审评中心(CDE)已于2017年5月将该药物的上市申请纳入优先审评程序。2018年2月13日,拜耳宣布CFDA已批准Eylea(阿柏西普眼内注射溶液)的上市申请,用于治疗成人糖尿病性黄斑水肿(DME)。
2020年,欧洲药品管理局(EMA)已批准了阿柏西普(艾力雅,通用名:aflibercept)新的预充式注射器,用于治疗5种成人视网膜疾病。
阿柏西普用法用量:(1)只为眼科玻璃体内注射。(2)阿柏西普的推荐剂量为2 mg (0.05 mL)给予通过玻璃体注射每4周(每月)对头3个月,接着2 mg (0.05 mL)通过玻璃体内注射每8周1次(2个月)。(3)尽管阿柏西普可能频如2 mg每4周给药(每月),当阿柏西普每4周给药与每8周比较时未显示增加疗效。 如发生严重出血、胃肠穿孔、伤口愈合不良、瘘管形成、高血压危象或高血压性脑病、动脉血栓、肾病综合征或血栓性微血管病、可逆性后部白质脑病综合征,应停药。
上一篇: 依普利酮治疗高血压的效果如何?
下一篇: 阿达木单抗注意事项
相关药讯
最新药讯

正品保障
正品保障 放心选购

厂家直采
厂家授权 正品渠道

专业药师
一对一用药指导

品类齐全
海外药房 药品齐全
微信客服
企业微信
联系我们 :24小时客服在线
400-001-2811

邮箱 : service@1blv.com
邮编 : 100096
地址 : 北京市昌平区珠江摩尔国际大厦3号楼2单元701室
本网站不销售任何药品,只做药品信息资讯展示
证书编号:(京)-非经营性-2020-0182 互联网药品信息服务资格证书














.png)
.png)