



Strensiq(阿法酸酶注射溶液)
Strensiq(阿法酸酶注射溶液)
通用名称:Strensiq
商品名称:Strensiq
英文名称:asfotase alfa
中文名称:阿法酸酶注射溶液
全部名称:Strensiq、asfotase alfa、阿法酸酶注射溶液
适应症
Strensiq(阿法酸酶注射溶液)适用于治疗围产期/婴儿期和青少年期磷酸酯酶过少症患者(HPP)。
剂型和规格
Strensiq(阿法酸酶注射溶液)是一种清澈、微乳白色或乳白色、无色至微黄色的水溶液;可能存在少量半透明或白色小颗粒。
该产品有以下几种规格:
1、18毫克/0.45毫升
2、28毫克/0.7毫升
3、40毫克/毫升
4、80毫克/0.8毫升
用法用量
1、围产期/婴儿发病HPP
Strensiq(阿法酸酶注射溶液)治疗围产期/婴儿期HPP的推荐剂量方案为每周皮下注射6毫克/千克,给药方式为:
1)每周3次,每次2毫克/千克,或
2)每周6次,每次1毫克/千克。注射部位反应可能会限制每周注射六次疗法的耐受性。
如果缺乏疗效(如呼吸状况、生长或影像学检查结果无改善),可将Strensiq(阿法酸酶注射溶液)的剂量增加至每周9毫克/千克,每周3次皮下注射3毫克/千克。
2、青少年发病HPP
Strensiq(阿法酸酶注射溶液)治疗青少年型HPP的推荐剂量方案为每周皮下注射6毫克/千克,给药方式为:
1)每周3次,每次2毫克/千克,或
2)每周6次,每次1毫克/千克。注射部位反应可能会限制每周注射六次疗法的耐受性。
3、制备和基于重量的剂量表
注意事项:不要将80毫克/0.8毫升的Strensiq(阿法酸酶注射溶液)小瓶用于体重低于40千克的儿科患者,因为使用80毫克/0.8毫升小瓶(较高浓度)的全身暴露量低于其他浓度小瓶(较低浓度)。对于这类患者,较低的暴露量可能无法满足这部分患者的需求。
1)根据患者的体重和推荐剂量确定处方剂量所需的每周总量。按照以下步骤确定患者剂量。
每周总剂量(毫克)=患者体重(千克)x处方剂量(毫克/千克/周)
每周总注射量(毫升)=总剂量(毫克/周)除以STRENSIQ浓度(40毫克/毫升或100毫克/毫升)。
每周样品瓶总数=总注射量除以样品瓶体积。
2)确定每周注射天数(每周3或6天)。
3)确定每日注射剂量。确定剂量时,患者体重应四舍五入至最接近的千克。使用下表作为指导,适用于每周三次给药2毫克/千克(表1)、每周六次给药1毫克/千克(表2)的患者,以及每周三次将剂量递增至3毫克/千克的患者,建议仅用于围产期/婴儿发作性HPP患者(表3)。
图1:每周3次2毫克/千克给药的体重剂量
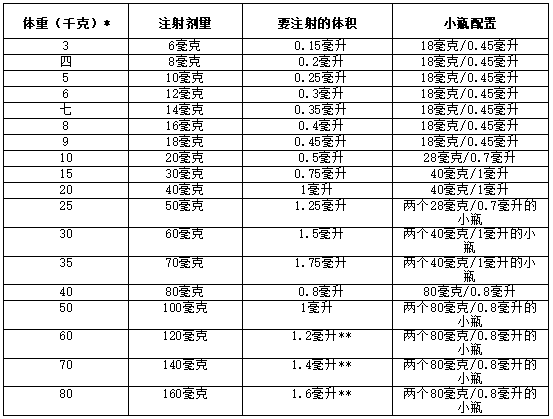
*不要将80毫克/0.8毫升的STRENSIQ小瓶用于体重低于40千克的儿童患者。
**准备大于1 mL的注射液时,在两个注射器之间等分注射液,并进行两次注射。进行两次注射时,使用两个独立的注射部位。
图2:每周6次1毫克/千克给药的体重剂量
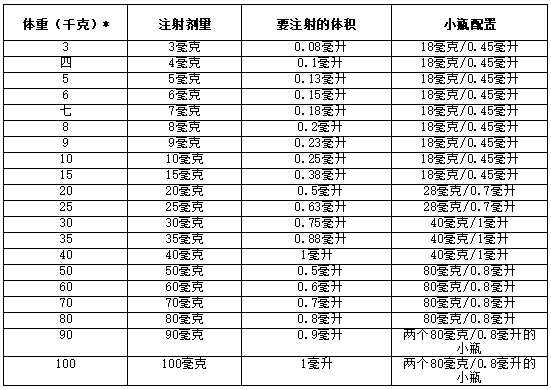
*不要将80毫克/0.8毫升的STRENSIQ小瓶用于体重低于40千克的儿童患者。
图3:每周3次给药3毫克/千克的体重剂量-仅适用于围产期/婴儿发病的HPP*
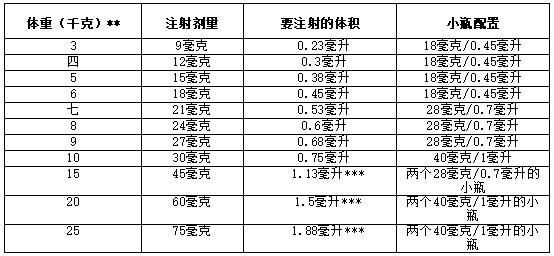
*仅建议围产期/婴儿期HPP患者采用每周三次每次3 mg/kg的给药方案。
**不要将80毫克/0.8毫升的STRENSIQ小瓶用于体重低于40千克的儿童患者。
***准备大于1 mL的注射液时,在两个注射器之间等分注射液,并注射两次。进行两次注射时,使用两个独立的注射部位。
4、注射前15至30分钟,将未开封的Strensiq(阿法酸酶注射溶液)小瓶从冰箱中取出,使液体达到室温。不要以任何其他方式加热Strensiq(阿法酸酶注射溶液),例如,不要在微波炉或热水中加热。
5、检查小瓶中的溶液是否有颗粒物质和变色。Strensiq(阿法酸酶注射溶液)为透明、微乳白色或乳白色、无色至微黄色水溶液;可能存在一些小的半透明或白色颗粒。
6、组装注射用品。使用一次性无菌1毫升注射器和 ½ 英寸注射针头注射 Strensiq(阿法酸酶注射溶液),建议使用25至29号针头。较大口径的针头(如25号)用于抽取药物,较小口径的针头(如29号)进行注射。如果剂量大于1毫升,注射量应平均分配到两个1毫升注射器均分。每次注射都要使用新的注射器和针头。
7、取下瓶盖,在无菌条件下准备小瓶,将注射器插入小瓶中,抽取处方剂量进行给药。不要摇晃。
8、消除注射器中的气泡并确认剂量是否正确。
9、Strensiq(阿法酸酶注射溶液)小瓶仅供一次性使用。未使用的产品请丢弃。
不良反应
1、常见不良反应:注射部位反应(63%)、脂肪营养不良(28%)、异位钙化(14%)和超敏反应(12%)。
2、不太常见的不良反应(发生率低于1%):低血钙症、肾结石、慢性肝炎、维生素B6减少。
注意事项
1、过敏反应
1)呼吸困难、窒息感、恶心、眶周水肿和头晕。这些反应在皮下注射Strensiq(阿法酸酶注射溶液)后几分钟内发生,并在治疗开始后超过1年后观察到。
2)其他过敏反应,包括呕吐、发热、头痛、潮红、易怒、寒战、红斑、皮疹、瘙痒和口腔感觉减退。
如果出现严重的过敏反应,应停止使用Strensiq(阿法酸酶注射溶液)并开始适当的药物治疗。如果决定重新给药,应监测患者是否再次出现严重过敏反应的体征和症状。
2、脂肪营养不良
使用Strensiq(阿法酸酶注射溶液)治疗的患者数月后在注射部位出现局部脂肪营养不良,包括脂肪萎缩和脂肪肥大。建议患者遵循正确的注射技术并轮换注射部位。
3、异位钙化
HPP患者发生异位钙化的风险增加。包括眼部(结膜和角膜)和肾脏(肾钙质沉着症、肾结石)。建议在使用Strensiq(阿法酸酶注射溶液)治疗期间定期进行眼科检查和肾脏超声检查,以监测眼部和肾脏异位钙化的体征和症状以及视力或肾功能的变化。
4、可能的免疫介导临床效应
在临床试验中,大多数接受Strensiq(阿法酸酶注射溶液)治疗的患者产生了抗asfotase alfa抗体和中和抗体,从而减少了asfotase alfa的全身暴露量。一些接受Strensiq(阿法酸酶注射溶液)治疗的患者最初有治疗反应,但随后出现复发和病情恶化,与疾病相关的实验室和放射学生物标志物表明免疫介导对Strensiq(阿法酸酶注射溶液)的药理作用会导致疾病进展。
特殊人群用药
1、妊娠期
尚无关于妊娠期患者使用Strensiq(阿法酸酶注射溶液)的可用数据来说明药物相关风险。在动物实验中,在器官形成期对怀孕大鼠和兔子静脉注射asfotase alfa,在导致血浆暴露的剂量分别为人体推荐剂量的21倍和24倍时,未发现胎儿毒性、胚胎致死性或致畸性的证据。
2、哺乳期
尚无关于母乳中是否存在α-硫胺素、对母乳喂养婴儿的影响或对乳汁产量的影响的数据。
3、儿童使用
使用Strensiq(阿法酸酶注射溶液)治疗围产期/婴儿期和青少年期HPP的安全性和有效性已在儿科患者中得到证实。
5、老年用药
尚无年龄在65岁以上的HPP 患者参与临床试验。因此,尚无资料证实65岁及以上的患者与年轻患者的反应是否不同。
药物相互作用
干扰实验室检测
1、利用碱性磷酸酶作为检测试剂的实验室检测
研究表明,Strensiq(阿法酸酶注射溶液)和利用碱性磷酸酶(ALP)结合检测系统的实验室检测之间存在分析干扰,从而导致接受Strensiq(阿法酸酶注射溶液)治疗的患者出现错误的检测结果。因此,建议在检测正在接受Strensiq(阿法酸酶注射溶液)治疗的患者的样本时使用不含碱性磷酸酶结合技术的实验室检测。为避免出现错误结果,请告知实验室操作人员患者正在接受Strensiq(阿法酸酶注射溶液)治疗。
2、血清碱性磷酸酶
通过实验室检测到高血清碱性磷酸酶测量值出现在接受Strensiq(阿法酸酶注射溶液)治疗的患者中,并反映了asfotase alfa的循环浓度。建议不要依赖血清ALP测定来为接受Strensiq(阿法酸酶注射溶液)治疗的患者做出临床决策。
成分
Strensiq(阿法酸酶注射溶液)的成分为:
1、活性成分:asfotase alfa。
2、非活性成分:磷酸氢二钠,七水合物;磷酸二氢钠、一水合物和氯化钠。
性状
注射液
贮存方法
1、Strensiq(阿法酸酶注射溶液)小瓶必须在2°C至8°C的冷藏条件下保存在原纸箱中,直到使用时为止,并避光保存。
2、从冰箱中取出后,Strensiq(阿法酸酶注射溶液)应在3小时内使用。
3、请勿在纸箱上标注的有效期后使用。
4、不要冷冻或摇晃。
5、小瓶仅供一次性使用。未使用的产品请丢弃。
生产厂家
亚力兄制药











 医伴旅服务热线:
医伴旅服务热线:








