


格卡瑞韦/哌仑他韦(glecaprevir/pibrentasvir)
格卡瑞韦/哌仑他韦(glecaprevir/pibrentasvir)
通用名称:glecaprevir/pibrentasvir
商品名称:Maviret
英文名称:glecaprevir/pibrentasvir
中文名称:格卡瑞韦/哌仑他韦
全部名称:格卡瑞韦/哌仑他韦、艾诺全、Maviret、glecaprevir/pibrentasvir
适应症
格卡瑞韦/哌仑他韦适用于治疗患有慢性丙型肝炎病毒(HCV)基因型1、2、3、4、5或6感染、无肝硬化或代偿性肝硬化(Child-Pugh A)的3岁及以上成人和儿童患者。
格卡瑞韦/哌仑他韦适用于治疗3岁及以上HCV基因型1感染的成人和儿童患者,这些患者以前接受过含HCV NS5A抑制剂或NS3/4A蛋白酶抑制剂(PI)的治疗方案,但未同时接受这两种治疗。
剂型和规格
格卡瑞韦/哌仑他韦为口服片剂或颗粒剂。
片剂:粉红色,长圆形,薄膜包衣,一面有 "NXT "字样。每片含100毫克格卡瑞韦和40毫克哌仑他韦。
口服颗粒:粉色和黄色包衣颗粒,单位剂量包装。每包含50毫克格卡瑞韦和20毫克哌仑他韦。
用法用量
1、治疗开始前的检测
在开始使用格卡瑞韦/哌仑他韦进行 HCV 治疗之前,通过测量乙型肝炎表面抗原 (HBsAg) 和乙型肝炎核心抗体 (anti-HBc) 来检测所有患者当前或既往的HBV感染证据。
2、3岁及以上患者的建议治疗时间
下表根据HCV单感染和HCV/HIV-1合并感染的代偿性肝病(有或没有肝硬化)和有或没有肾功能损害的患者(包括接受透析的患者)的患者人群提供了推荐的格卡瑞韦/哌仑他韦治疗持续时间。
表:未接受过任何“针对该病症”的治疗的病人的建议持续时间

表:接受过治疗的患者的建议持续时间
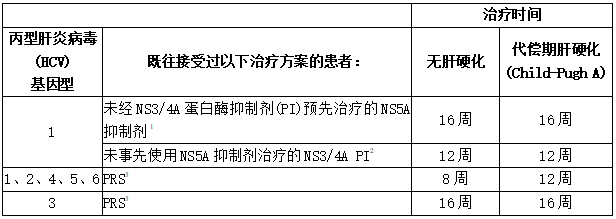
1.在临床试验中,受试者接受先前的含莱地帕病毒和索非布韦的治疗方案,或达卡他韦联合(peg)干扰素和利巴韦林的治疗方案。
2.在临床试验中,受试者接受了含有西美普韦和索非布韦,或西美普韦、波切韦和泰拉韦联合(peg)干扰素和利巴韦林的既往治疗方案。
3.PRS=既往接受过含有(peg)干扰素、利巴韦林和/或索非布韦的治疗方案,但未接受过 HCV NS3/4A PI 或 NS5A 抑制剂的治疗。
3、成人推荐剂量
格卡瑞韦/哌仑他韦剂是一种固定组合药物产品,每片含有100毫克格卡瑞韦和40毫克哌仑他韦。
成年人格卡瑞韦/哌仑他韦的推荐口服剂量为3片,与食物同时服用,每日一次(每日总剂量:格卡瑞韦300毫克和哌仑他韦120毫克)。
4、3岁及以上儿童患者的推荐剂量
3岁至12岁以下儿童患者使用格卡瑞韦/哌仑他韦的推荐剂量以体重为依据。建议3至12岁体重低于45千克的儿童患者服用格卡瑞韦/哌仑他韦口服颗粒。袋装格卡瑞韦/哌仑他韦口服颗粒是一种固定组合药物产品,每包中含有50毫克格卡瑞韦和20毫克哌仑他韦。
12岁及以上的儿童患者或体重至少45千克的儿童患者服用格卡瑞韦/哌仑他韦的建议剂量是,与食物同时服用三片,每日一次(每日总剂量:300毫克格卡瑞韦和120毫克哌仑他韦)。
下表所示为儿科患者的剂量。
表:3岁及以上儿童患者的推荐剂量
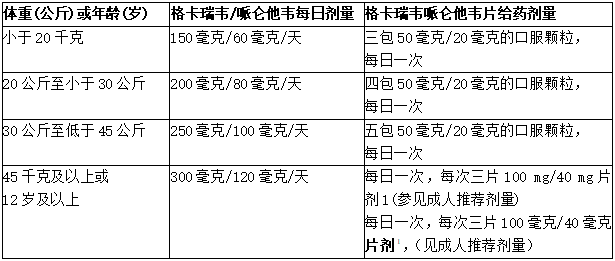
1.体重45千克及以上且无法吞咽片剂的儿童患者可每日一次服用六包50毫克/20毫克口服颗粒。尚未对体重超过45千克的儿童患者进行口服颗粒给药的研究。
5、口服颗粒的制备和给药
1)口服颗粒应与食物一起服用,每日一次。此外,每日总剂量的口服颗粒应洒在少量含水量低的软食上,软食可能粘在汤匙上,无需咀嚼即可吞咽(如花生酱、巧克力榛子酱、奶油奶酪、浓果酱或希腊酸奶)。
2)食物和口服颗粒的混合物应在配制后15分钟内全部吞下;口服颗粒不应碾碎或咀嚼。
3)不建议使用会从汤匙上滴下或滑落的液体或食物,因为药物可能会快速溶解并降低效力。
6、肝移植或肾移植受者
对于3岁及以上接受肝脏或肾脏移植的患者,建议使用格卡瑞韦/哌仑他韦12周。对于未经NS3/4A蛋白酶抑制剂预先治疗而接受NS5A抑制剂治疗的基因型1感染患者或接受PRS治疗的基因型3感染患者,建议治疗期为16周。
7、肝功能损害
中度或重度肝功能损害(Child- Pugh B或C)或有任何既往肝功能代偿不全史的患者禁用格卡瑞韦/哌仑他韦。
不良反应
1、严重副作用:
1)乙型肝炎病毒再激活
2)在开始格卡瑞韦/哌仑他韦治疗前有或有晚期肝脏问题的患者中:肝脏问题恶化、肝功能衰竭和死亡的罕见风险:
a.恶心、腹泻、疲倦、混沌、嗜睡、呕血、头晕
b.皮肤发黄或眼睛发白
c.胃上腹部(腹部)肿胀或疼痛
d.食欲不振
e.深色或棕色(茶色)尿液、深色、黑色或带血的大便
2、常见的副作用(大于10%):头痛和疲倦。
注意事项
1、HCV与HBV病毒合并感染患者的乙型肝炎病毒再激活风险
有报告称,正在接受或已完成HCV直接作用抗病毒药物治疗但未接受HBV抗病毒治疗的HCV/HBV合并感染患者中出现了乙型肝炎病毒(HBV)再活现象。一些病例导致了暴发性肝炎、肝功能衰竭和死亡。在HBsAg阳性的患者和血清学证据显示HBV感染已解除(即HBsAg阴性和抗HBc阳性)的患者中也有病例报告。在接受某些免疫抑制剂或化疗药物治疗的患者中也有HBV再激活的报道;这些患者在接受HCV直接作用抗病毒药物治疗时发生HBV再激活的风险可能会增加。
HBV再激活的特点是HBV复制突然增加,表现为血清HBV DNA水平迅速升高。在HBV感染缓解的患者中,可能会再次出现HBsAg。HBV复制再活化可能伴有肝炎,即转氨酶水平升高,严重时胆红素水平升高、肝衰竭和死亡。
在开始使用格卡瑞韦/哌仑他韦进行HCV治疗之前,通过检测HBsAg和抗HBc,检测所有患者是否存在当前或既往HBV感染证据。对于有HBV感染血清学证据的患者,在使用格卡瑞韦/哌仑他韦进行HCV治疗期间和治疗后随访期间,应监测肝炎复发或HBV再激活的临床和实验室迹象。根据临床指征启动适当的HBV感染患者管理。
2、有晚期肝病证据的患者出现肝功能失代偿/衰竭的风险
据报道,在接受包括格卡瑞韦/哌仑他韦在内的含HCV NS3/4A蛋白酶抑制剂方案治疗的患者中,出现了肝功能失调/衰竭的上市后病例,其中包括致命病例。由于这些事件是从规模不确定的人群中自愿报告的,因此并不总是能够可靠地估计其发生频率或确定与药物暴露的因果关系。
大多数出现严重后果的患者在开始接受格卡瑞韦/哌仑他韦治疗前已患有中度或重度肝功能损害(Child-Pugh B 或 C)的晚期肝病,包括一些据报道基线时患有轻度肝功能损害(Child-Pugh A)的代偿性肝硬化,但之前出现过失代偿事件(即之前有腹水、静脉曲张出血、脑病病史)的患者。无肝硬化或代偿性肝硬化(Child-Pugh A)患者出现肝功能失代偿/衰竭的病例极少;其中许多患者有门脉高压的证据。同时服用不建议合用药物的患者,或有严重肝脏相关内科或外科并发症等混杂因素的患者也发生了此类事件。病例通常发生在治疗的前 4 周内(中位数为 27 天)。
对于代偿性肝硬化(Child-PughA))或有门脉高压等晚期肝病证据的患者,根据临床需要进行肝实验室检测;并监测肝失代偿的体征和症状,如存在黄疸、腹水、肝性脑病和静脉曲张出血。对出现肝失代偿/肝衰竭证据的患者停止治疗。
中度至重度肝功能损害(ChildPugh B 或 C)或曾有肝功能失代偿病史的患者禁用格卡瑞韦/哌仑他韦。
3、格卡瑞韦/哌仑他韦与卡马西平、含有依非韦伦的治疗方案或圣约翰草同时使用导致治疗效果降低的风险
卡马西平、依非韦伦和圣约翰草可能会显著降低格卡瑞韦和哌仑他韦的血浆浓度,从而降低格卡瑞韦/哌仑他韦的治疗效果。不建议将这些药物与 MAVYRET 同时使用。
特殊人群用药
1、妊娠期
目前尚无足够的人类数据来确定格卡瑞韦/哌仑他韦是否会对妊娠结果造成风险。在动物生殖研究中,在器官发育期分别给药格卡瑞韦/哌仑他韦的各成分,其暴露量最高为格卡瑞韦/哌仑他韦推荐剂量下人类暴露量的53倍或51倍和1.5倍时,未观察到不良发育影响。在动物体内无法就格卡瑞韦可能对发育产生的影响得出明确结论,因为该物种体内格卡瑞韦的最高暴露量仅为推荐剂量下人类暴露量的7%(0.07倍)。在啮齿类动物产前/产后发育研究中,两种化合物均未产生影响,在这些研究中,母体对格卡瑞韦和哌仑他韦的全身暴露量(AUC)分别约为推荐剂量下人体暴露量的47倍和74倍。
适用人群出现重大出生缺陷和流产的背景风险尚不清楚。在美国普通人群中,临床确认的妊娠中重大出生缺陷和流产的背景风险估计分别为2%至4%和15%至20%。
2、哺乳期
尚不清楚格卡瑞韦/哌仑他韦的成分是否会排泄到母乳中、影响母乳产量或对母乳喂养的婴儿产生影响。当对动物给药时,格卡瑞韦/哌仑他韦的成分存在于乳汁中,对哺乳幼仔中观察到的生长和发育没有影响。
在考虑母乳喂养对发育和健康的益处的同时,还应考虑母亲对格卡瑞韦/哌仑他韦的临床需求以及格卡瑞韦/哌仑他韦或潜在母体疾病对母乳喂养的儿童的任何潜在不良影响。
3、儿童使用
对于12岁及以上或体重至少45千克的儿童患者,无需调整格卡瑞韦/哌仑他韦的剂量。3岁至12岁以下儿童患者服用格卡瑞韦/哌仑他韦的推荐剂量是根据体重确定的。
在HCV GT1、2、3或4感染的3岁及以上儿童患者中,格卡瑞韦/哌仑他韦的安全性、疗效和药代动力学基于127名3岁至18岁无肝硬化受试者的开放标签试验数据,这些受试者为未经治疗(n=114)或接受过治疗(n=13)并接受了格卡瑞韦/哌仑他韦 8、12或16周(DORA-第1部分和第2部分)。在3岁至18岁以下受试者中观察到的不良反应与在成年人中进行的格卡瑞韦/哌仑他韦临床试验中观察到的不良反应一致,但呕吐、皮疹和上腹痛除外,与成年人相比,在12岁以下儿童受试者中观察到的频率更高。
本试验观察到的疗效结果与格卡瑞韦/哌仑他韦在成人中的临床试验观察到的结果一致。
在患有肝硬化、有肾脏和/或肝脏移植史或感染HCV GT5或6的儿童患者中,观察到儿童受试者与成人受试者的格卡瑞韦和哌仑他韦暴露相当,这证明了格卡瑞韦/哌仑他韦的安全性和有效性。
4、老年用药
在格卡瑞韦/哌仑他韦临床试验中,328名受试者年龄为65岁及以上(占2期和3期临床试验受试者总数的14%),47名受试者年龄为75岁及以上(2%)。在这些受试者和较年轻受试者之间未观察到安全性或有效性的总体差异,其他已报告的临床经验未发现老年受试者和较年轻受试者之间的应答差异。无需在老年患者中调整格卡瑞韦/哌仑他韦的剂量。
5、肾功能损害
对于轻度、中度或重度肾功能损害的患者,包括正在透析的患者,无需调整格卡瑞韦/哌仑他韦的剂量。
6、肝功能损害
对于轻度肝功能损害的患者,无需调整格卡瑞韦/哌仑他韦的剂量(Child-Pugh A)。尚未对格卡瑞韦/哌仑他韦进行评估,在HCV感染的中度或重度肝功能损害(Child-Pugh B或Child-Pugh C)患者或有任何既往肝功能代偿不全病史的患者中禁用格卡瑞韦/哌仑他韦。这些患者中曾报告过上市后肝失代偿/衰竭病例。严重肝功能损害(Child-Pugh C)的受试者中格利卡韦和皮布伦他韦的暴露量均较高。
7、注射吸毒者(PWID)和因阿片类药物使用障碍而接受药物辅助治疗(MAT)的人
在PWID或因阿片类药物使用障碍而接受MAT治疗的患者中,不需要调整格卡瑞韦/哌仑他韦的剂量。在格卡瑞韦/哌仑他韦临床试验中,自我认定为当前/最近PWID的受试者、前PWID受试者和未报告注射用药史的受试者之间的安全性和疗效相似。报告合用MAT治疗阿片类药物使用障碍的受试者与未报告合用MAT的受试者之间,格卡瑞韦/哌仑他韦的安全性和疗效也相似。
禁忌症
1、中度或重度肝功能损害(Child-Pugh B 或 C)患者或曾有肝功能失代偿病史者禁用格卡瑞韦/哌仑他韦。
2、格卡瑞韦/哌仑他韦禁止与阿扎那韦或利福平同时用药。
药物相互作用
1、格卡瑞韦/哌仑他韦对其他药物潜在作用机制
格卡瑞韦和哌仑他韦是P-糖蛋白(P-gp)、乳腺癌抗性蛋白(BCRP)和有机阴离子转运多肽(OATP)1B1/3的抑制剂。与格卡瑞韦/哌仑他韦联合用药可能会增加作为P-gp、BCRP、OATP1B1 或 OATP1B3 底物的药物的血浆浓度。格卡瑞韦和哌仑他韦是细胞色素P450 (CYP)3A、CYP1A2 和尿苷葡萄糖醛酸转移酶 (UGT) 1A1的弱抑制剂。
2、其他药物对格卡瑞韦/哌仑他韦的潜在作用机制
格卡瑞韦和哌仑他韦是P-gp和/或BCRP的底物。格卡瑞韦是OATP1B1/3的底物。将格卡瑞韦/哌仑他韦与抑制肝P-gp、BCRP或OATP1B1/3的药物联合用药可能会增加格卡瑞韦和/或哌仑他韦的血浆浓度。
将格卡瑞韦/哌仑他韦与诱导P-gp/CYP3A的药物联合用药可能会降低格卡瑞韦和哌仑他韦的血浆浓度。
卡马西平、苯妥英、依非韦伦和圣约翰草可能会显著降低格卡瑞韦和哌仑他韦的血浆浓度,从而降低格卡瑞韦/哌仑他韦的治疗效果。不建议将这些药物与格卡瑞韦/哌仑他韦同时使用。
3、已确定的和其他潜在的药物相互作用
使用直接作用抗病毒药物清除 HCV 感染可能会导致肝功能发生变化,从而影响同时用药的安全性和有效性。例如,在上市后病例报告和已发表的流行病学研究中,糖尿病患者的血糖控制发生改变,导致严重的症状性低血糖。
在这些病例中,处理低血糖症需要停用或调整用于治疗糖尿病的伴随药物的剂量。
建议经常监测相关实验室参数(如服用华法林的患者的国际标准化比值 [INR]、糖尿病患者的血糖水平)或同时服用的药物浓度,如治疗指数较窄的 CYP P450 底物(如某些免疫抑制剂),以确保用药安全有效。可能需要调整同时服用药物的剂量。
下表列出了格卡瑞韦/哌仑他韦对合用药物浓度的影响,以及合用药物对格卡瑞韦和哌仑他韦的影响。所有相互作用研究均在成人中进行。
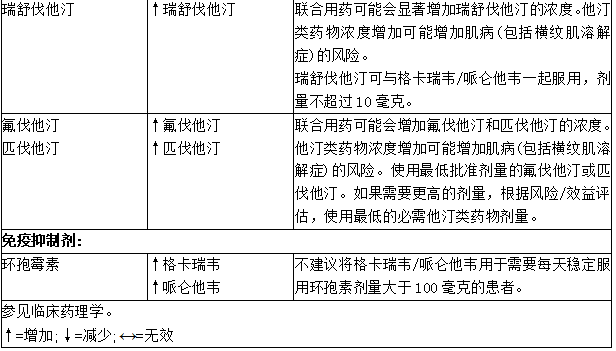
表:药物相互作用研究中发现的潜在重大药物相互作用
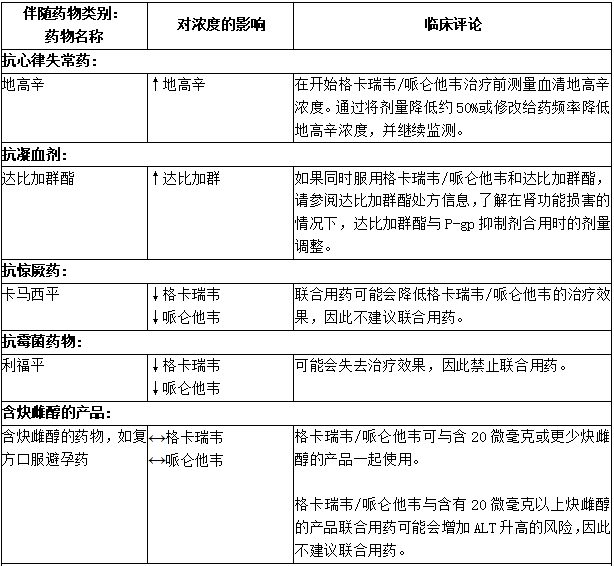
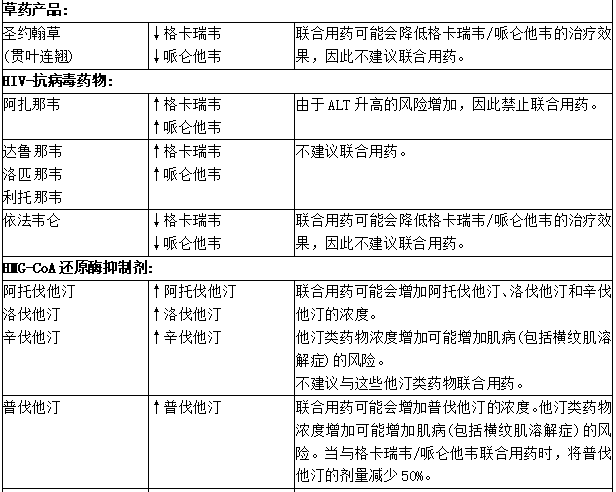
4、阿片类药物使用障碍的药物辅助治疗(MAT)
与格卡瑞韦/哌仑他韦同时使用时,无需调整丁丙诺啡/纳洛酮或美沙酮的剂量。关于纳曲酮与格卡瑞韦/哌仑他韦同时使用的建议,目前尚无足够的信息。
5、与格卡瑞韦/哌仑他韦无明显临床相互作用的药物
当格卡瑞韦/哌仑他韦与下列药物同时服用时,无需调整剂量:阿巴卡韦, 氨氯地平, 咖啡因, 右美沙芬, 多鲁曲韦, 艾维曲韦/可比司他, 恩曲他滨, 20微克或以下的炔雌醇, 非洛地平, 拉米夫定, 拉莫三嗪, 洛沙坦, 咪达唑仑、炔诺酮或其他仅含孕激素的避孕药、奥美拉唑、雷替格韦、利匹韦林、索非布韦、他克莫司、替诺福韦丙烯酰胺、富马酸替诺福韦二吡呋酯、托布他胺和缬沙坦。
药物过量
如果格卡瑞韦/哌仑他韦用药过量,应监测患者的任何毒性体征和症状。应立即进行适当的对症治疗。血液透析对格卡瑞韦和哌仑他韦清除效果不明显。
成分
1、格卡瑞韦/哌仑他韦片剂
有效成分:格卡瑞韦和哌仑他韦
非活性成分:胶体二氧化硅、共聚维酮(K 28型)、交联羧甲基纤维素钠、羟丙甲纤维素2910、氧化铁红、一水乳糖、聚乙二醇3350、丙二醇单辛酸酯(II型)、硬脂富马酸钠、二氧化钛和维生素E(生育酚)聚乙二醇琥珀酸酯。这种药片不含麸质。
2、格卡瑞韦/哌仑他韦口服颗粒:
有效成分:格卡瑞韦和哌仑他韦
非活性成分:胶体二氧化硅、共聚维酮(K 28型)、交联羧甲基纤维素钠、羟丙甲纤维素2910、氧化铁红、氧化铁黄、一水乳糖、聚乙二醇/聚乙二醇3350、丙二醇单辛酸酯(II型)、硬脂富马酸钠、二氧化钛、维生素E(生育酚)聚乙二醇琥珀酸酯。口服颗粒不含谷蛋白。
性状
片剂、口服颗粒剂
贮存方法
1、将格卡瑞韦/哌仑他韦储存在30°C或以下。
2、将格卡瑞韦/哌仑他韦保存在其原始包装中,直到准备使用。
3、将格卡瑞韦/哌仑他韦和所有药物放在儿童拿不到的地方
生产厂家
艾伯维









 医伴旅服务热线:
医伴旅服务热线:








