



康奈非尼(BRAFTOVI、Encorafenib)
康奈非尼(BRAFTOVI、Encorafenib)
通用名称:Encorafenib
商品名称:BRAFTOVI
英文名称:Encorafenib
中文名称:康奈非尼
全部名称:康奈非尼、恩考芬尼、恩可非尼、BRAFTOVI、Encorafenib
适应症
1、BRAF V600E或V600K突变阳性不可切除或转移性黑色素瘤
经FDA批准的检测,康奈非尼(BRAFTOVI、Encorafenib)适用于与比美替尼联合治疗BRAF V600E或V600K突变的不可切除或转移性黑色素瘤患者。
2、BRAF V600E突变阳性转移性结直肠癌(CRC)
康奈非尼(BRAFTOVI、Encorafenib)适用于与西妥昔单抗联合治疗成年转移性结直肠癌(CRC)患者,该患者在既往治疗后出现BRAF V600E突变(经FDA批准的检测检测)。
3、BRAF V600E突变阳性转移性非小细胞肺癌(NSCLC)
经FDA批准的检测,康奈非尼(BRAFTOVI、Encorafenib)适用于与比美替尼联合治疗BRAF V600E突变的成人转移性非小细胞肺癌(NSCLC)患者。
4、使用限制
康奈非尼(BRAFTOVI、Encorafenib)不适用于野生型BRAF黑色素瘤、野生型BRAF CRC或野生型BRAF非小细胞肺癌患者的治疗。
适应靶点
BRAF
剂型和规格
胶囊:75毫克,硬明胶,米色瓶盖上有 "A"字样,白色瓶身上有 "LGX 75 毫克"字样。
用法用量
1、患者选择
1)BRAF V600E或V600K突变阳性不可切除或转移性黑色素瘤
在开始康奈非尼(BRAFTOVI、Encorafenib)治疗之前,确认肿瘤标本中是否存在BRAF V600E或V600K突变。
2)BRAF V600E突变阳性转移性结直肠癌(CRC)
在开始康奈非尼(BRAFTOVI、Encorafenib)治疗之前,确认肿瘤标本中是否存在BRAF V600E突变。
3)BRAF V600E突变阳性转移性非小细胞肺癌(NSCLC)
在开始康奈非尼(BRAFTOVI、Encorafenib)治疗之前,确认肿瘤或血浆标本中是否存在BRAF V600E突变。
2、BRAF V600E或V600K突变阳性的不可切除或转移性黑色素瘤以及BRAF V600E突变阳性的转移性非小细胞肺癌的推荐剂量(NSCLC)
康奈非尼(BRAFTOVI、Encorafenib)的推荐剂量为450毫克(六粒75毫克胶囊),口服,每日一次,与比美替尼联合用药,直至疾病进展或出现不可接受的毒性。有关推荐的比美替尼剂量信息,请参阅比美替尼处方信息。
3、BRAF V600E突变阳性转移性结直肠癌(CRC)的推荐剂量
康奈非尼(BRAFTOVI、Encorafenib)的推荐剂量为300毫克(四粒75毫克胶囊),口服,每日一次,与西妥昔单抗联合用药,直至疾病进展或出现不可接受的毒性。有关西妥昔单抗的推荐给药信息,请参阅西妥昔单抗处方信息。
4、管理
康奈非尼(BRAFTOVI、Encorafenib)可与食物同服或不同服。请勿在下次给药后12小时内补服。
如果康奈非尼(BRAFTOVI、Encorafenib)给药后出现呕吐,请勿再服用一剂,但应继续服用下一预定剂量。
5、不良反应剂量调整
1)BRAF V600E或V600K突变阳性不可切除或转移性黑色素瘤或BRAF V600E突变-阳性转移性非小细胞肺癌
如果停用比美替尼,则将康奈非尼(BRAFTOVI、Encorafenib)降至最大剂量300毫克(四粒75毫克胶囊),每日一次,直至恢复使用比美替尼。
与康奈非尼(BRAFTOVI、Encorafenib)相关的不良反应的剂量减少情况见下表。
表:因不良反应而建议减少康奈非尼(BRAFTOVI、Encorafenib)的剂量-黑色素瘤或非小细胞肺癌

2)BRAF V600E 基因突变阳性的转移性结直肠癌 (CRC)
如果停用西妥昔单抗,则停用康奈非尼(BRAFTOVI、Encorafenib)。
与康奈非尼(BRAFTOVI、Encorafenib)相关的不良反应的剂量减少情况见下表。
表:因不良反应而建议减少康奈非尼(BRAFTOVI、Encorafenib)的剂量-转移性结直肠癌

3)BRAF V600E或V600K突变阳性不可切除或转移性黑色素瘤,BRAF V600E突变阳性转移性结直肠癌(CRC),或BRAF V600E突变阳性非小细胞肺癌
与康奈非尼(BRAFTOVI、Encorafenib)相关的不良反应的剂量调整见下表。
表:康奈非尼(BRAFTOVI、Encorafenib)不良反应建议剂量调整
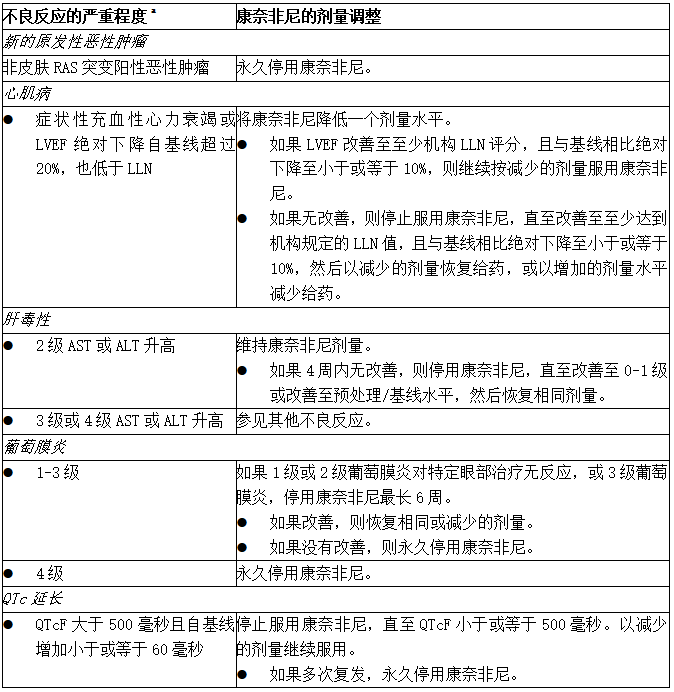
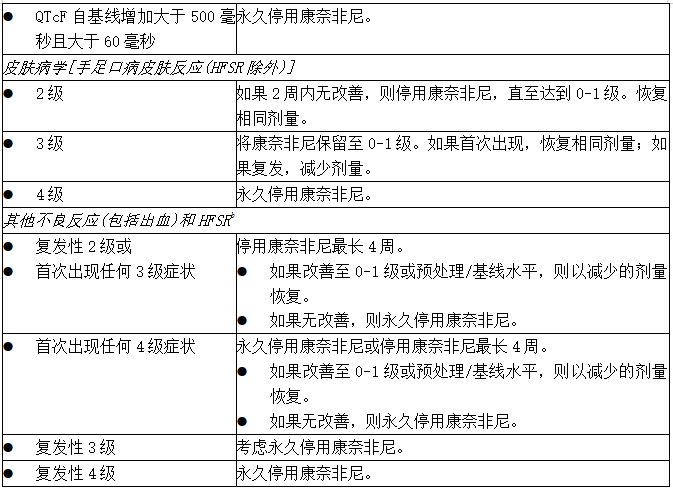
a 美国国家癌症研究所不良事件通用术语标准(NCI ctae)第4.03版。
b 对于新的原发性皮肤恶性肿瘤,当与比美替尼或西妥昔单抗联合用药时,不建议对康奈非尼(BRAFTOVI、Encorafenib)进行剂量调整;除葡萄膜炎、虹膜炎和虹膜睫状体炎以外的眼部事件;间质性肺病/肺炎;肌酸磷酸激酶(CPK)升高;横纹肌溶解症;和静脉血栓栓塞。
有关与每种产品相关的不良反应的剂量调整,请参考比美替尼或西妥昔单抗处方信息(如适用)。
6、与强效或中度CYP3A4抑制剂联合用药的剂量调整
避免将康奈非尼(BRAFTOVI、Encorafenib)与强效或中度CYP3A4抑制剂联合用药。如果不能避免同时服用,则根据下表中的建议减少康奈非尼(BRAFTOVI、Encorafenib)的剂量。在抑制剂停用3至5个消除半衰期后,恢复开始CYP3A4抑制剂之前服用的康奈非尼(BRAFTOVI、Encorafenib)剂量。
表:与强效或中度CYP3A4抑制剂联合用药时,康奈非尼(BRAFTOVI、Encorafenib)的推荐剂量减少量

a 当前日剂量是指基于适应症的康奈非尼(BRAFTOVI、Encorafenib)建议剂量,或基于表1(黑色素瘤)和表2(CRC)中的给药建议的不良反应减少量。
b 当与强效CYP3A4抑制剂联合用药时,75毫克QD康奈非尼(BRAFTOVI、Encorafenib)剂量的Encorafenib暴露量预计会高于不含CYP3A4抑制剂时150毫克QD剂量的暴露量,且与不含CYP3A4抑制剂时225毫克QD剂量的暴露量相似。当使用150毫克剂量水平的康奈非尼(BRAFTOVI、Encorafenib)联合强效CYP3A4抑制剂时,密切监测患者的不良反应并进行临床判断。
不良反应
1、严重副作用
1)新的原发性恶性肿瘤
2)BRAF野生型肿瘤中的肿瘤促进
3)心肌病
4)肝毒性
5)出血
6)葡萄膜炎
7)QT延长
8)胚胎-胚儿毒性
9)与康奈非尼(BRAFTOVI、Encorafenib)单一药剂相关的风险
10)联合用药相关风险
2、康奈非尼(BRAFTOVI、Encorafenib)与比美替尼联合用药治疗黑色素瘤时,最常见的副作用包括:乏力、恶心、呕吐、腹痛、关节疼痛或肿胀(关节痛)。
3、康奈非尼(BRAFTOVI、Encorafenib)与西妥昔单抗联合用药治疗结直肠癌时,最常见的副作用包括:疲劳、胃区(腹部)疼痛、恶心、食欲减退、腹泻、关节疼痛或肿胀(关节痛)、痤疮样皮疹、皮疹。
4、康奈非尼(BRAFTOVI、Encorafenib)与比美替尼联合用药治疗非小细胞肺癌时,最常见的副作用包括:疲劳、视力模糊、视力丧失或其他视力改变、恶心、便秘、腹泻、气促、肌肉或关节痛、皮疹、呕吐、咳嗽、胃区(腹部)疼痛。
注意事项
1、新的原发恶性肿瘤
在接受BRAF抑制剂治疗的患者中观察到了新的皮肤和非皮肤原发性恶性肿瘤,而且康奈非尼(BRAFTOVI、Encorafenib)也可能发生这种情况。
1)皮肤恶性肿瘤
在COLUMBUS中,在接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者中,包括角化棘皮瘤(KA)在内的皮肤鳞状细胞癌(cuSCC)发生率为2.6%,基底细胞癌发生率为1.6%。首次出现cuSCC/KA的中位时间为5.8个月(范围为1至9个月)。
在接受康奈非尼(BRAFTOVI、Encorafenib)单药治疗的患者中,报告cuSCC/KA的患者占8%,报告基底细胞癌的患者占1%,报告新发原发性黑色素瘤的患者占5%。
在BEACON CRC中,1.4%的CRC患者出现cuSCC/KA,1.4%接受康奈非尼(BRAFTOVI、Encorafenib)联合西妥昔单抗治疗的患者出现新的原发性黑色素瘤。
在PHAROS中,在接受 康奈非尼(BRAFTOVI、Encorafenib) 联合比美替尼治疗的患者中,cuSCC和皮肤乳头状瘤各占2%。
开始治疗前、治疗期间每2个月以及停止治疗后最长6个月进行一次皮肤病学评估。通过切除和皮肤病理学评估管理可疑的皮肤病变。不建议对新的原发性皮肤恶性肿瘤进行剂量调整。
2)非皮肤恶性肿瘤
根据其作用机制,康奈非尼(BRAFTOVI、Encorafenib)可能通过突变或其他机制促进与RAS激活相关的恶性肿瘤。监测接受康奈非尼(BRAFTOVI、Encorafenib)治疗的患者非皮肤恶性肿瘤的体征和症状。对于RAS突变阳性的非皮肤恶性肿瘤,停用康奈非尼(BRAFTOVI、Encorafenib)。
2、BRAF野生型肿瘤中的肿瘤促进
体外实验证明,在暴露于BRAF抑制剂的BRAF野生型细胞中,MAP激酶信号传导会被激活,细胞增殖也会增加。在开始使用康奈非尼(BRAFTOVI、Encorafenib)之前,请确认BRAF V600E或V600K突变的证据。
3、心肌症
在接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者中,曾报告出现心肌病,表现为左心室功能障碍伴有症状性或无症状性射血分数降低。在COLUMBUS中,7%接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者出现心肌病证据(LVEF的减少低于机构LLN,LVEF的绝对减少≥10%,通过超声心动图或MUGA检测)。1.6%的患者出现3级左心室功能障碍。接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者首次出现左心室功能障碍(任何级别)的中位时间为3.6个月(范围为0至21个月)。87%接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者心肌病消退。
在PHAROS中,接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者中有11%出现心肌病迹象(LVEF下降至机构LLN以下,LVEF绝对下降≥10%,通过超声心动图或MUGA检测)。1%的患者出现3级左心室功能障碍。82%接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者心肌病消退。
在开始治疗前、开始治疗后一个月以及治疗期间每2至3个月通过超声心动图或MUGA扫描评估射血分数。在基线射血分数低于50%或低于机构规定的正常下限(LLN)的患者中,尚未确定康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼的安全性。使用康奈非尼(BRAFTOVI、Encorafenib)治疗时,应密切监测有心血管风险因素的患者。
根据不良反应的严重程度,暂停、减少剂量或永久停用。
4、肝中毒
当康奈非尼(BRAFTOVI、Encorafenib)与比美替尼联合给药时,可能发生肝毒性。在COLUMBUS中,接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者中,丙氨酸转氨酶(ALT)升高3级或4级的发生率为6%,天冬氨酸转氨酶(AST)升高2.6%,碱性磷酸酶升高0.5%。在PHAROS中,接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者中,AST的肝功能实验室检测出现3级或4级升高的发生率为10%,ALT为9%,碱性磷酸酶为3.2%。
在开始康奈非尼(BRAFTOVI、Encorafenib)治疗前监测肝脏实验室检测,在治疗期间每月监测一次,并根据临床指示进行监测。根据不良反应的严重程度,暂停、减少剂量或永久停用。
5、出血
在COLUMBUS中,19%接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者发生出血;3.2%的患者出现3级或以上出血。最常见的出血事件为胃肠道事件,包括直肠出血(4.2%)、便血(3.1%)和痔出血(1%)。1.6%的患者在出现新的或进行性脑转移时发生致命性颅内出血。
在BEACON CRC中,19%接受康奈非尼(BRAFTOVI、Encorafenib)联合西妥昔单抗治疗的患者发生出血;1.9%的患者发生3级或以上出血,其中0.5%的患者发生致死性消化道出血。最常见的出血事件为鼻出血(6.9%)、便血(2.3%)和直肠出血(2.3%)。
在PHAROS中,12%接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者发生出血,包括致命性颅内出血(1%);4.1%的患者发生3级或4级出血。最常见的出血事件为肛门出血和血胸(各2%)。
根据不良反应的严重程度,暂停、减少剂量或永久停用。
6、葡萄膜炎
在接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者中,曾有发生葡萄膜炎(包括虹膜炎和虹膜睫状体炎)的报告。在COLUMBUS中,康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者葡萄膜炎的发生率为4%。在PHAROS中,康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者葡萄膜炎的发生率为1%。
每次就诊时评估视觉症状。定期进行眼科评估,以发现新的或恶化的视觉障碍,并跟踪新的或持续的眼科检查结果。根据不良反应的严重程度,暂停、减少剂量或永久停用。
7、QT延长
在一些患者中,康奈非尼(BRAFTOVI、Encorafenib)与剂量依赖性QTc间期延长有关。在COLUMBUS中,0.5%(1/192)接受康奈非尼(BRAFTOVI、Encorafenib)与比美替尼联用治疗的患者测得QTcF升高至 >500毫秒。在PHAROS中,2.1%(2/95)接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者测得 QTcF 升高至 >500 毫秒。
监测已经发生QTc延长或有发生QTc延长重大风险的患者,包括已知长QT综合征、有临床意义的缓慢性心律失常、严重或无法控制的心力衰竭以及服用其他与QT延长相关的药物的患者。纠正康奈非尼(BRAFTOVI、Encorafenib)给药前和给药期间的低钾血症和低镁血症。在QTc >500毫秒内停用、减少剂量或永久停用。
8、胚胎-胎儿毒性
根据其作用机制,对孕妇使用康奈非尼(BRAFTOVI、Encorafenib)可对胎儿造成伤害。Encorafenib在动物中引起胚胎-胎儿发育变化,在大于或等于推荐剂量450毫克导致暴露量约为人暴露量的26倍和178倍的剂量下,在较高剂量中为堕胎药,在较低剂量下未见明显发现。
告知孕妇和有生殖潜力的女性对胎儿的潜在风险。建议有生殖潜力的女性使用有效的非激素避孕方法,因为康奈非尼(BRAFTOVI、Encorafenib)在治疗期间和最后一次给药后2周内会使激素避孕药无效。
9、与康奈非尼(BRAFTOVI、Encorafenib)作为单一药物相关的风险
与康奈非尼(BRAFTOVI、Encorafenib)与比美替尼联合使用相比,康奈非尼(BRAFTOVI、Encorafenib)作为单一药物使用时会增加某些不良反应的风险。在COLUMBUS中,21%使用康奈非尼(BRAFTOVI、Encorafenib)单剂治疗的患者发生3级或4级皮肤反应,而使用康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的患者发生2%的皮肤反应。
如果比美替尼被暂时中断或永久停用,则按照建议减少康奈非尼(BRAFTOVI、Encorafenib)的剂量。
10、联合治疗相关风险
康奈非尼(BRAFTOVI、Encorafenib)适用于与比美替尼或西妥昔单抗联合用药。有关其他风险信息,请参阅比美替尼和西妥昔单抗的处方信息。
特殊人群用药
1、妊娠期
根据其作用机制,对孕妇给予康奈非尼(BRAFTOVI、Encorafenib)可对胎儿造成伤害。目前尚无妊娠期间使用康奈非尼(BRAFTOVI、Encorafenib)的临床数据。在动物生殖研究中,encorafenib在动物中引起胚胎-胎儿发育变化,在大于或等于临床剂量450毫克时导致暴露量约为人暴露量的26倍和178倍的剂量下,encorafenib在178倍剂量下是一种堕胎药,但在较低剂量时没有明确发现。告知孕妇和有生殖潜力的女性对胎儿的潜在风险。
2、哺乳期
关于encorafenib或其代谢产物在人乳中的存在、对母乳喂养的婴儿的影响或对产奶量的影响,目前尚无相关数据。由于康奈非尼(BRAFTOVI、Encorafenib)母乳喂养的儿童可能出现严重的不良反应,建议妇女在康奈非尼(BRAFTOVI、Encorafenib)治疗期间和最后一次给药后2周内不要进行母乳喂养。
3、具有生殖潜力的男性和女性
对孕妇服用康奈非尼(BRAFTOVI、Encorafenib)可对胎儿造成伤害。
在开始康奈非尼(BRAFTOVI、Encorafenib)治疗之前,验证具有生殖潜力的女性的妊娠状态。
告知有生殖潜力的女性在康奈非尼(BRAFTOVI、Encorafenib)治疗期间和末次给药后2周内使用有效避孕方法。建议患者使用非激素避孕方法,因为康奈非尼(BRAFTOVI、Encorafenib)可能会使激素避孕药无效。
根据在剂量约为450毫克临床剂量下人暴露量13倍的雄性动物中的发现,使用康奈非尼(BRAFTOVI、Encorafenib)可能会影响雄性动物的生育力。
4、儿童用药
尚未确定康奈非尼(康奈非尼(BRAFTOVI、Encorafenib)、Encorafenib)在儿科患者中的安全性和有效性。
5、老年用药
在多个临床试验中接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的690例BRAF突变阳性黑色素瘤患者中,20%的患者年龄在65至74岁之间,8%的患者年龄在75岁及以上。
在216例接受康奈非尼(BRAFTOVI、Encorafenib)联合西妥昔单抗治疗的BRAF V600E突变阳性转移性CRC患者中,62例(29%)为65岁至75岁,20例(9%)为75岁及以上。
在接受康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼治疗的98例BRAF V600E突变阳性非小细胞肺癌转移性患者中,62例(63%)为65岁及以上,20例(20%)为75岁及以上。
与年轻患者相比,未在老年患者中观察到康奈非尼(BRAFTOVI、Encorafenib)联合比美替尼或康奈非尼(BRAFTOVI、Encorafenib)联合西妥昔单抗的安全性或有效性的总体差异。
6、肾功能损害
对于轻度至中度肾功能损害(CLcr 30至<90毫升/分钟)的患者,不建议调整康奈非尼(BRAFTOVI、Encorafenib)剂量。严重肾功能损害(CLcr <30毫升/分钟)患者的推荐剂量尚未确定。
7、肝功能损害
对于轻度肝功能损害(Child-Pugh A类)的患者,不建议调整康奈非尼(BRAFTOVI、Encorafenib)剂量。尚未确定中度(Child-Pugh B类)或重度(Child-Pugh C类)肝功能损害患者的推荐剂量。
药物相互作用
1、敏感CYP3A4底物
康奈非尼(BRAFTOVI、Encorafenib)在稳态下是一种强效CYP3A4诱导剂。康奈非尼(BRAFTOVI、Encorafenib)联合用药可能会降低CYP3A4底物(包括激素类避孕药)的血浆浓度,这可能会降低这些底物的疗效。避免与CYP3A4底物合用康奈非尼(BRAFTOVI、Encorafenib),因为血浆浓度降低可能导致底物药效降低。如果无法避免同时给药,请参阅CYP3A4底物产品标签中的建议。
2、OATP1B1、OATP1B3或BCRP基底
康奈非尼(BRAFTOVI、Encorafenib)与OATP1B1、OATP1B3或BCRP底物联合给药会导致底物浓度增加,并可能增加这些药物的毒性。联合用药时,密切监测患者暴露量增加的体征和症状,并考虑调整这些底物的剂量。
3、延长QT间期的药物
康奈非尼(BRAFTOVI、Encorafenib)与剂量依赖性QTc间期延长有关。避免将康奈非尼(BRAFTOVI、Encorafenib)与已知会延长QT/QTc间隔时间的药物联合用药。
药物过量
由于encorafenib与血浆蛋白的结合率为86%,因此血液透析在治疗康奈非尼(BRAFTOVI、Encorafenib)用药过量时可能无效。
成分
活性成分:encorafenib
非活性成分:共聚维酮、泊洛沙姆188、微晶纤维素、琥珀酸、交聚维酮、胶体二氧化硅和植物来源的硬脂酸镁
胶囊壳:明胶、二氧化钛、氧化铁红、氧化铁黄、氧化铁红、单印油墨(药用釉、氧化铁、丙二醇)
性状
胶囊剂
贮存方法
1、储存在20°C至25°C的室温下。
2、将康奈非尼(BRAFTOVI、Encorafenib)保存在原装瓶中。
3、将康奈非尼(BRAFTOVI、Encorafenib)瓶紧紧地封闭,并防止受潮。
4、康奈非尼(BRAFTOVI、Encorafenib)附带一个干燥剂包在瓶子里,以帮助保护您的药物免受水分。不要从瓶中取出干燥剂包。
5、将康奈非尼(BRAFTOVI、Encorafenib)和所有药物放在儿童拿不到的地方。
生产厂家
辉瑞

















 医伴旅服务热线:
医伴旅服务热线:








